43/2003. (IV. 26.) FVM rendelet
43/2003. (IV. 26.) FVM rendelet
a takarmányok előállításáról, forgalomba hozataláról és felhasználásáról szóló 2001. évi CXIX. törvény végrehajtásáról1
A takarmányok előállításáról, forgalomba hozataláról és felhasználásáról szóló 2001. évi CXIX. törvény (a továbbiakban: Tv.) 18. §-ának a)–l) pontjában kapott felhatalmazás alapján – a b) pont esetén a gazdasági és közlekedési miniszterrel egyetértésben, a c) pont esetén az egészségügyi, szociális és családügyi miniszterrel egyetértésben – a következőket rendelem el:
(A Tv. 2. §-ához)
1. § E rendelet alkalmazásában:
1. A Tv. 2. §-ának 5. pontja szerinti előkeverékek csoportjai:
a) vitamin premix: vitamin(ok) és készítménye(ik) vivőanyaggal alkotott keveréke,
b) mikroelem premix: mikroelem(ek) és készítménye(ik) vivőanyaggal alkotott keveréke,
c) egységes premix: vitamin és mikroelem-készítmények vivőanyaggal alkotott keveréke, amely állatgyógyászati készítményeket, valamint egyéb takarmány-adalékanyagot is tartalmazhat,
d) komplett premix: vitamin-, mikroelem-, továbbá makroelem-készítmények vivőanyaggal alkotott keveréke, amely egyéb takarmány-adalékanyagokat és állatgyógyászati készítményeket is tartalmazhat,
e) koncentrátum: vitamin-, mikroelem-, makroelem-készítmények, fehérjetakarmányok keveréke, amely takarmány-adalékanyagot és állatgyógyászati készítményeket is tartalmazhat,
f) gyógypremix: állatgyógyászati készítmény vivőanyaggal alkotott keveréke.
2.2 Etethetőségi/felhasználhatósági, illetve minőségmegőrzési idő: a takarmány-előállító üzem által a gyártás időpontjától számított időtartam alapján megállapított időpont, ameddig az előállított takarmány, a takarmány-előállító üzem által előírt tárolási feltételek mellett, megőrzi fizikai, kémiai, érzékszervi jellemzőit és kifogásmentes mikrobiológiai állapotát.
3. Gazdasági haszonállat: az emberek által élelmiszer, prém, gyapjú, toll és bőrtermelés, sporttevékenység, illetve igaerő céljából etetett, tartott állat.
4. Élelmiszer-termelő állat: az emberek által élelmiszer vagy élelmiszer-alapanyag előállítás céljából etetett és tartott gazdasági haszonállat.
5.3 Kedvtelésből tartott állat: a prémes állatok kivételével olyan fajhoz tartozó állat, amely faj egyedeit az ember táplálja és tartja, de nem fogyasztja.
6. Laboratóriumi állat: laboratóriumi kísérletek céljából tartott és takarmányozott állat.
7. Takarmány engedélyezése: az engedélyezésre bejelentett új takarmány takarmányozási célú alkalmasságának, illetve a gyártó által megnevezett hasznosíthatóságának megállapítása a benyújtott dokumentumok, valamint laboratóriumi vizsgálatok és az eddigiektől eltérő új előállítási eljárás ismeretében, a szükség szerint elvégzett állatetetési, illetve kihasználási kísérletek alapján.
8. Tétel:
a) gyártási tétel:
aa) egy keverési mennyiség a szakaszos technológiával előállított takarmánykeverék és előkeverék esetében, ha az egyes keverési mennyiségek egymástól azonosíthatóan elkülöníthetőek,
bb) az a takarmánymennyiség, amelyet ugyanabban az üzemben, ugyanazon a munkanapon, műszakban és gépen, azonos összetétellel és beltartalommal, azonos néven állítanak elő;
b) kereskedelmi tétel:
ba) egy adott takarmány tároló helyre szállított és ott tárolt azonos elnevezésű, jelölésű, előállítási helyű, idejű és gyártási tételszámú takarmánymennyiség,
bb) takarmány forgalmazó helyen található azonos elnevezésű, jelölésű, előállítási helyű, idejű és gyártási tételszámú takarmánymennyiség.
9. A vizsgált tétellel azonos takarmány: az a tétel, amelyből a mintát vették, és amelyre a minta vizsgálatának eredményei vonatkoznak.
10. Tételszám: a gyártási tétel azonosítási száma.
11. Termékszám: a gyártmánylapon és a Magyarországon előállított takarmánykeverék, előkeverék jelölésén feltüntetett, azonosítást szolgáló szám.
12. Mintavételi alap: az a takarmánymennyiség, amelyből a mintát vették, és amelyre a minta vizsgálati eredményei vonatkoznak.
13. Közvetítő: aki az előállítás és a felhasználás közötti szakaszban a takarmány tárolását, illetve forgalomba hozatalát végzi.
14. Engedélyköteles takarmányvizsgáló laboratórium: a takarmányozási hatóságok, a kutatási, oktatási intézmények takarmányvizsgáló laboratóriuma, és a szolgáltatási tevékenységet végző takarmányvizsgáló laboratórium.
15. Referencia laboratórium: a takarmányok teljes körű érzékszervi, fizikai, kémiai-analitikai és mikrobiológiai vizsgálatainak elvégzésére alkalmas laboratórium, amely végzi a laboratóriumok engedélyezéséhez szükséges minősítő vizsgálatokat, a laboratóriumok közti összehasonlításokat, a laboratóriumok ellenőrzését, illetve jártassági és módszeregyeztető körvizsgálatokat szervez.
16. Laboratóriumok közti összehasonlítás: a vizsgálati minták két vagy több laboratórium között meghatározott feltételek szerint elvégzendő vizsgálatainak megszervezése, végrehajtása és a vizsgálati eredmények értékelése.
17. Körvizsgálatok:
a) jártassági körvizsgálat: az az eljárás, amely során minimum 10 laboratórium vizsgálati eredményeinek összehasonlításával és statisztikai módszerek felhasználásával történő értékeléssel meghatározzák az egyes laboratóriumok vizsgálati teljesítményét, vizsgálati adataik következetességét és összevethetőségét, adott vizsgálati spektrumban való megfelelőségét,
b) módszeregyeztető körvizsgálat: egy adott vizsgálati módszer meghatározott feltételek szerinti, minimum 8 laboratórium részvételével lefolytatott körvizsgálata, amely a metodika vizsgálati eredményeinek reprodukálhatóságát határozza meg.
18. Melaszos takarmány: melasz felhasználásával előállított, legalább 14%, szacharózban kifejezett összcukrot tartalmazó kiegészítő takarmány.
19. Probiotikum: az állatok bélflóra egyensúlyának megteremtésére és stabilizálására, valamint a takarmányok biológiai tartósítására alkalmas, hasznos mikroorganizmus(oka)t tartalmazó készítmény.
20. Mikrobiológiai eredetű enzimek: mikroorganizmusok által termelt, nagy molekulatömegű fehérjék, amelyek az állatok tápcsatornájába jutva a tápláló anyagok lebontását, emésztését a biokémiai reakció sebességének fokozásával segítik.
21. Kritikus pontok: a takarmány minőségét és biztonságát leginkább veszélyeztető pontok a takarmányok előállításának, tárolásának, feldolgozásának, szállításának, exportjának, importjának, tranzitjának, felhasználásának területén.
22.4 Állat: olyan fajhoz tartozó állat, amely faj egyedeit az ember táplálja, tartja vagy fogyasztja.
23.5 Genetikailag módosított takarmány: a genetikailag módosított élelmiszerekről és takarmányokról szóló, az Európai Parlament és a Tanács 1829/2003/EK rendelete (a továbbiakban: 1829/2003/EK rendelet) 2. cikkének 7. pontja szerint genetikailag módosított takarmány.
(A Tv. 4. §-ához)
2. § (1)6 A takarmány-előállító üzemnek a működési engedély iránti kérelmét – a külön jogszabály szerinti használatbavételi engedély megadását követően – a takarmány-előállító üzem fekvése szerint illetékes megyei (fővárosi) állategészségügyi és élelmiszer-ellenőrző állomáshoz (a továbbiakban: Állomás) kell benyújtania. A kérelemhez csatolni kell az Állatgyógyászati Oltóanyag-, Gyógyszer- és Takarmány-ellenőrző Intézet (a továbbiakban: ÁOGYTI) állásfoglalás iránti kérelmet az 1. számú melléklet szerint.
(2)7 Az ÁOGYTI állásfoglalását a 2. számú melléklet, illetve a Magyar Takarmánykódex kötelező előírásairól szóló jogszabály (a továbbiakban: Takarmánykódex) 6. számú melléklete szerint alakítja ki. Az állásfoglalásnak tartalmaznia kell a halliszt felhasználásra vonatkozó véleményt is.
(3) Az ÁOGYTI-nek a tanúsított minőségbiztosítási, minőségügyi és biztonsági rendszerrel – pl. ISO 9001:2000, GMP, illetve HACCP – rendelkező takarmány-előállító üzem minőség-ellenőrzési szabályzatának értékelése során figyelembe kell vennie ezen rendszerek működését.
3. § (1)8 Az új takarmány-előállító üzemnek az ÁOGYTI állásfoglalásához szükséges próbagyártáshoz engedélyt kell beszereznie. Az engedélyt az Állomás adja ki, megjelölve a próbagyártás időtartamát.
(2) Az Állomás a próbagyártás során előállított takarmányok forgalomba hozatalát és felhasználását az általa meghatározott laboratóriumi vizsgálatok eredményeinek ismeretében engedélyezheti.
4. §9
5. § (1)10 Az Állomás a működési engedélyben meghatározza:
a) az előállítható takarmányok körét,
b)11
c) gyógyszeres takarmánykeverék előállítása esetén az állatgyógyászati készítmény(ek), illetve az az(oka)t tartalmazó előkeverékek legkisebb bekeverhető mennyiségét,
d) az állatgyógyászati készítmény(ek) előkeverékbe bekeverhető legkisebb mennyiségét,
e) az előállítható takarmányokban a felhasználásra kerülő állatgyógyászati készítmény(ek) hatóanyag-tartalmának alsó és felső határértékeit,
f) a takarmány-előállítás során a legkisebb mennyiségben bekeverhető összetevő még homogénen elkeverhető tömegét,
g) az előállítás személyi és gyártástechnológiai feltételeit,
h) a takarmány-előállító üzem takarmány minőség- és biztonság-ellenőrzési rendszerének megfelelőségét,
i)12
(2) A működési engedélyben foglaltaktól való eltérés szándéka esetén új működési engedélyt kell kérni a 2–4. § és az (1) bekezdésben foglaltak szerint.
(3)13 A takarmány-előállító üzem működési engedélyét, annak lejárta előtt, meg kell újítani. Az erre irányuló kérelmet az Állomásnak a lejárat előtt legkésőbb 1 hónappal kell benyújtani. Az Állomás az engedélyt a 2–4. § és az (1) bekezdésben foglaltak szerint adja meg.
(4) A működési engedélyt vissza kell vonni, ha
a) a létesítmény megszünteti tevékenységét, vagy
b) az Állomás megállapítja, hogy a takarmány-előállító üzem tevékenysége a működési engedélyben foglalt, a takarmány minősége és biztonsága szempontjából lényeges követelménynek nem felel meg, és e követelményeknek a takarmány-előállító üzem az Állomás által megszabott határidőn belül nem tesz eleget.
6. §14 A takarmány tároló és forgalmazó helynek a Tv. 5. §-a (3) bekezdésének a) pontja és (4) bekezdésének a) pontja szerinti működési engedélye megadásánál az Állomás az állásfoglalását a Tv.-nek, e rendeletnek és a Takarmánykódex 6. számú mellékletének a tárolásra és forgalmazásra vonatkozó előírásainak figyelembevételével alakítja ki.
7. § (1) Az Állomás a működési engedéllyel rendelkező takarmány-előállító üzemekről és közvetítőkről nyilvántartást vezet.
(2) Az Állomások által megadott adatok alapján a működési engedéllyel rendelkező takarmány-előállító üzemek és közvetítők központi nyilvántartását és a Takarmánykódex 6. számú melléklete szerinti nyilvántartási számmal való ellátását az ÁOGYTI végzi.
(3) A nyilvántartási számmal rendelkező takarmány-előállító üzemek és közvetítők listáját a Földművelésügyi és Vidékfejlesztési Minisztérium (a továbbiakban: Minisztérium) hivatalos lapjában az ÁOGYTI évente közzéteszi.
(4) Az egyes kereskedelmi tevékenységek gyakorlásáról szóló jogszabályban foglalt termékek esetén a közvetítői tevékenység folytatásának feltétele, hogy a jogszabály szerint nyilvántartásba vételre jogosult szerv a közvetítőt és üzletét, raktárát vagy tárolóját nyilvántartásba vegye.
(5)15 Az ÁOGYTI az Európai Unió Bizottságának minden év december 31-éig megküldi a Takarmánykódex 6. számú melléklete A. részének I–IV. fejezete és B. részének I–II. fejezete szerinti, engedélyezett takarmány-előállító üzemek és közvetítők listáját.
(6)16 Az ÁOGYTI az Európai Unió tagállamainak minden év december 31-éig megküldi a Takarmánykódex 6. számú melléklete A. része I. fejezetének 1. pontja és A. része II. fejezetének 1. pontja, valamint a B. részének I. fejezete szerinti, engedélyezett takarmány-előállító üzemek és közvetítők listáját.
(7) Az ÁOGYTI az Európai Unió valamely tagállamának kérésére megküldi a Takarmánykódex 6. számú melléklete A. részének III. és IV. fejezete szerinti takarmány-előállító üzemek listáját, vagy annak a kért részét.
(8)17 Az Európai Unión kívüli országokból (a továbbiakban: harmadik ország) a Takarmánykódex 6. számú melléklete A. részének I.1., II.1., III.1., IV.1., V.1. a)–c) pontjában felsorolt takarmány-adalékanyag, állatok fehérje ellátásának javítására használható egyes termék, előkeverék és takarmánykeverék akkor hozható be Magyarországra, ha az azt előállító üzem rendelkezik Magyarországon a behozatalért felelős képviselővel.
(9)18 A magyarországi képviselőnek 2004. március 20-ig kell bejelenteni a székhelye szerint illetékes Állomás részére a takarmány-előállító üzem nevét, címét, és a takarmány-előállító üzemnek a Takarmánykódex 6. számú melléklete C. részének (2) lábjegyzete szerinti tevékenységét. Az ezt követően tevékenységét megkezdő képviselőnek az első behozatalt megelőző legkésőbb 14 nappal kell az Állomásnak a kért adatokat megadni. Az Állomás ezen adatokat az ÁOGYTI-nek 14 napon belül megküldi. Az ÁOGYTI a képviselőkről nyilvántartást vezet. E nyilvántartást a minisztériummal egyeztetve megküldi az Európai Unió Bizottságának és azokat évente a Földművelésügyi és Vidékfejlesztési Minisztérium Hivatalos Lapjában közzéteszi.
(10)19 A (9) bekezdés szerinti bejelentéssel egyidejűleg a képviselőnek nyilatkozatot kell benyújtania arról, hogy
a) vállalják annak biztosítását, hogy a harmadik ország takarmány-előállító üzeme megfelel a Takarmánykódex 6. számú mellékletében foglalt követelményeknek,
b) vezetik az általuk képviselt takarmány-előállító üzemek által Magyarországra behozott takarmányoknak a 6. számú melléklet szerinti nyilvántartásait.
(11)20 Az Állomás megtiltja azon harmadik országban működő takarmány-előállító üzemek termékeinek forgalomba hozatalát és felhasználását, amely képviselője nem teljesíti a (8) és (9) bekezdésben foglaltakat.
8. § (1) A takarmány-előállító üzemnek az előállítani kívánt takarmányról az előállítást megelőzően gyártmánylapot kell készítenie. A gyártmánylapon feltüntetendő adatokat a 3. számú melléklet tartalmazza. A gyártmánylapokat a gyártás befejezésétől számítva 5 évig meg kell őrizni.
(2)21 Kizárólag
a) a Takarmánykódex 1. és 14. számú melléklete szerinti, valamint az Európai Unió bármely tagállamában jogszerűen előállított, illetve forgalomba hozott takarmány-alapanyag,
b) a Takarmánykódex 4. számú melléklete szerinti takarmány-adalékanyag, továbbá
c) a 19. § (1) bekezdése szerint eseti jelleggel engedélyezett takarmány-alapanyag és -adalékanyag
állítható elő, – a 19. § (1) bekezdésének a) pontja kivételével – hozható forgalomba és használható fel.
(3) A takarmányokat kőolaj, kőolajipari melléktermékek elégetéséből származó füstgázokkal, füstgáz-levegő keverékeivel közvetlenül kezelni, szárítani tilos.
(4) A mikrobiológiai eredetű enzimkészítmények nem tartalmazhatják a kiindulási mikroorganizmusokat.
9. § (1) A Takarmánykódex 6. számú mellékletében meghatározott takarmány-előállító üzemeknek, takarmány tároló és forgalmazó helyeknek meg kell felelnie az ott meghatározott követelményeknek.
(2) A takarmányok forgalomba hozatalának feltételeire vonatkozó előírásokat a Takarmánykódex 7. számú melléklete tartalmazza.
(3)22 A részben vagy teljesen géntechnológiával módosított szervezetekből származó takarmányok nyomon követhetőségére a genetikailag módosított szervezetek nyomon követhetőségéről és jelöléséről, és a genetikailag módosított szervezetekből származó élelmiszerek és takarmányok nyomon követhetőségéről, valamint a 2001/18/EK irányelv módosításáról szóló, az Európai Parlament és a Tanács 1830/2003/EK rendeletének előírásait alkalmazni kell.
10. § (1) A takarmány-előállítás feltétele a 4. számú mellékletben felsorolt nyilvántartások pontos vezetése.
(2) A forgalomba hozatal céljából takarmányt előállító üzemnek és a közvetítőnek a panaszok nyilvántartására és elintézésére rendszert kell kialakítania.
(3) A forgalomba hozatal céljából takarmányt előállító üzemnek és a közvetítőnek a nyomon követhetőség biztosítására olyan nyilvántartást kell vezetnie, amelynek segítségével a termék súlyos minőséghiba, illetve takarmány biztonsági probléma esetén a forgalomból azonnal visszahívható. A visszahívott termék további sorsát, az azzal kapcsolatos hatósági intézkedéseket dokumentálni kell. A visszahívott terméknek ismételt forgalomba helyezése előtt hatósági minőség-ellenőrzési és biztonsági felülvizsgálat alá kell esnie.
(4) A minőség-ellenőrzési szabályzatban előírt feladatok napi végrehajtásáról a takarmány-előállító üzemnek minőség-ellenőrzési naplót kell vezetni. A napló vezetésének elvégzésére felelős személyt kell kijelölni. A tanúsított minőségbiztosítási, minőségügyi és biztonsági rendszerrel – pl. ISO 9001:2000, GMP, illetve HACCP – rendelkező takarmány-előállító üzem esetén nem kell minőség-ellenőrzési naplót vezetni, ha e rendszerek nyilvántartásai megfelelnek a minőség-ellenőrzési naplónak.
(5) A takarmány-előállító üzem köteles megőrizni a végzett ellenőrzések eredményeit oly módon, hogy a dokumentáció alkalmas legyen a takarmány minden tétele előállítási folyamatának nyomon követésére és forgalomba hozatalra szánt takarmánynál panasz esetén a felelősség megállapítható legyen.
11. §23 (1) Az állati eredetű fehérjék takarmányozási célú felhasználására a fertőző szivacsos agyvelőbántalmak megelőzéséről, az ellenük való védekezésről, illetve leküzdésükről szóló jogszabály rendelkezéseit kell alkalmazni.
(2) A kérődző állatok takarmányainak előállítását az Állomásnak meg kell tiltania az olyan takarmány-előállító üzem esetében, amely az (1) bekezdés szerinti rendelet előírásai közül megszegi
a) a kérődző állatok takarmányának a nem kérődző élelmiszertermelő állatok takarmányaitól elkülönült gyártására vonatkozó rendelkezéseket, illetve
b) a kérődző állatok takarmányainak – az üzem által végeztetett – tételes laboratóriumi vizsgálatára vonatkozó rendelkezést, ha kérődző és nem kérődző élelmiszertermelő állatok takarmányának előállítása ugyanabban az üzemben történik.
(3) Ha a (2) bekezdés b) pontja szerinti laboratóriumi vizsgálat kedvező eredménye alapján az üzem által forgalomba hozatalra vagy felhasználásra felszabadított tételből a hatósági ellenőrzés során vett minta laboratóriumi vizsgálata tiltott állati eredetű fehérjét mutat ki, akkor az Állomásnak – a tétel kérődzőkkel való felhasználásának megtiltása mellett – a kérődző állatok takarmányainak gyártását meg kell tiltania és az esetet ki kell vizsgálnia. A vizsgálatnak minden esetben ki kell terjednie az üzem alapanyag és gyártás-technológiai nyilvántartásának ellenőrzésre, valamint az alapanyagok laboratóriumi vizsgálatára.
(4) Az Állomás a kérődző állatok takarmányainak gyártására vonatkozó tilalmat visszavonja, ha
a) a (2) bekezdés a) pontjában említett rendelkezéseknek az üzem újra megfelel, illetve írásban nyilatkozik arról, hogy a b) pont rendelkezéseit is betartja, továbbá bemutatja a vizsgálatok végzésére jogosult laboratóriummal megkötött megállapodást, kivéve, ha az üzem saját laboratóriuma is jogosult a vizsgálatok elvégzésére, vagy
b) az Állomás által a (3) bekezdés alapján végzett vizsgálat kimutatja, hogy a tiltott állati eredetű fehérjével való szennyeződés veszélye nem áll fenn.
(5) Az (1) bekezdés szerinti rendeletnek az élelmiszertermelő állatok takarmányainak a nem élelmiszer termelő állatok takarmányaitól elkülönült előállítására vonatkozó előírásai megszegése esetén az élelmiszer-termelő állatok takarmányainak előállítását az Állomásnak meg kell tiltania. Az Állomás a tilalmat akkor vonja vissza, ha az üzem újra megfelel az (1) bekezdés szerinti rendelet előírásainak.
(6) Ha a takarmány-előállító üzem az Állomásnak a (2), (3) vagy (5) bekezdés alapján hozott tiltása ellenére továbbra is előállít kérődzőknek, illetve élelmiszertermelő állatoknak szánt takarmányt, akkor az Állomás a 38. § (3) bekezdés c) pontjában foglaltak szerint jár el.
(7) Új takarmány-előállító üzemnek működési engedély csak akkor adható, ha a fertőző szivacsos agyvelőbántalmak megelőzéséről, az ellenük való védekezésről, illetve leküzdésükről szóló jogszabály előírásainak a létesítendő üzem megfelel.
11/A. §24 (1)25 Az Állomás – a kizárólag kérődző állatok takarmányaiban megengedett állati eredetű fehérjét felhasználó takarmány-előállító üzemek kivételével – nyilvántartásba veszi azokat a takarmány-előállító üzemeket, amelyekben állati eredetű fehérjék élelmiszertermelő állatok takarmányaiban való felhasználását engedélyezte.
(2) A takarmány-előállító üzemek az (1) bekezdés szerinti nyilvántartás elkészítése és vezetése során kötelesek – a nyilvántartásban foglalt adataik változásáról történő haladéktalan értesítésre is kiterjedően – együttműködni az Állomással.
(3) Az Állomás a nyilvántartás változásáról az ÁOGYTI-t haladéktalanul értesíti, amely a változást az országos nyilvántartásban átvezeti.
(4) Az ÁOGYTI a takarmány-előállító üzemek országos nyilvántartásáról és annak változásairól a minisztériumot folyamatosan és haladéktalanul tájékoztatja.
(5)26 A (4) bekezdés szerinti nyilvántartást az ÁOGYTI a minisztérium jóváhagyását követően küldi meg az Európai Unió Bizottsága és az Európai Unió többi tagállama részére.
12. § (1) Gyógyszeres takarmányt csak olyan takarmány-előállító üzem állíthat elő, amelynek a működési engedélye ezt lehetővé teszi.
(2)27
(3) A gyógyszeres takarmány előállítása kizárólag állatorvos szakmai felügyeletével történhet. Az állatorvos szakmai felügyelete az állatgyógyászati készítmények beszerzésének, tárolásának, jelölésének, folyamatos felhasználásának, az erre vonatkozó dokumentumoknak, továbbá a gyógyszeres takarmány gyártmánylapjának ellenőrzésére terjed ki.
(4) A takarmány-előállító üzem részére beszerzendő állatgyógyászati készítményt, illetve a gyógyszeres takarmánynak minősülő előkeveréket az állatorvos a vénykiállításra vonatkozó szabályok szerint rendeli meg. A gyógyszeres takarmánykeverék előállításához szükséges állatorvosi rendelvényt (a továbbiakban: rendelvény) az 5. számú melléklet, kiállításának feltételeit külön jogszabály tartalmazza. A rendelvény érvényességi ideje legfeljebb harminc nap.
(5) A rendelvényt három példányban kell kiállítani. A rendelvény egy példánya az állatorvosnál marad, második példányát a takarmány-előállító üzem, harmadik példányát az állattartó kapja. A rendelvényt három évig kell megőrizni. A takarmány-előállító üzemnél a három évet a gyógyszeres takarmány kiadásától kell számítani.
(6) A takarmány-előállító üzemben felhasználásra kerülő gyógyszereket és gyógypremixeket külön erre a célra szolgáló helyiségben (gyógyszerszoba) kell tárolni, külön jogszabály előírása szerint.
(7) Vényköteles állatgyógyászati készítményt tartalmazó gyógyszeres takarmányt csak a gyártó, illetve az állatgyógyászati készítmények forgalmazásra jogosult hozhat forgalomba.
(8) A Takarmánykódex 4. számú mellékletének II. 1. pontja szerinti állatgyógyászati készítményekre a (7) bekezdésben foglaltak nem vonatkoznak.
13. § (1) A takarmány tároló és forgalmazó helyen a takarmányokat egymástól a keveredés, átszennyeződés lehetőségének kizárásával, jól láthatóan elkülönítve, megjelölve kell tárolni.
(2) A gyógyszeres takarmányokat az egyéb takarmányoktól elkülönítve, megjelölve kell tárolni.
(3) A takarmány tároló és forgalmazó helyen az állatra vagy az emberre nézve mérgező vagy ártalmas, illetve a tárolt takarmány minőségét károsan befolyásoló anyag nem tárolható.
(4) Zsákban tárolt takarmányokat csak száraz padozatú, hűvös helyen, padozattal és oldalfalakkal nem érintkező módon – a szellőzés biztosításával – szabad tárolni.
(5) A tárolás során biztosítani kell a takarmány minősége és biztonsága megóvásának feltételeit, és be kell tartani az előállító által előírt tárolási feltételeket.
14. § (1) A Takarmánykódex 3. számú mellékletében felsorolt tiltott anyagokat, illetve ilyen anyagokat tartalmazó takarmányokat takarmányozási célra felhasználni tilos.
(2) A tiltott anyagokat tartalmazó takarmányt a további előállításból, forgalmazásból, az exportból, importból, a felhasználásból, a szállításból az előállítónak, a forgalmazónak, az importőrnek és a felhasználónak ki kell vonni az Állomás egyidejű értesítése mellett.
(3) A (2) bekezdés szerint kivont takarmány megsemmisítését a környezetvédelmi és vám előírások figyelembevételével az Állomás elrendeli. A megsemmisítő helyre való szállítást az Állomás engedélyezi.
15. § (1) A Takarmánykódex 2. számú mellékletében foglalt megengedhető mennyiségeknél nagyobb mértékben nemkívánatos anyagot tartalmazó takarmányt, annak megállapításával egyidejűleg, a további előállításból, forgalmazásból, az exportból, importból, a felhasználásból, a szállításból az előállítónak, az importőrnek, a forgalmazónak és a felhasználónak, az Állomás egyidejű értesítése mellett, ki kell vonnia.
(2)28 Amennyiben a nemkívánatos anyagot a megengedettnél nagyobb mértékben tartalmazó takarmányt az Állomás részére az (1) bekezdés alapján bejelentik, illetve az Állomás ellenőrzése során valamely takarmányról azt állapítja meg, hogy az nemkívánatos anyagot a megengedettnél nagyobb mértékben tartalmaz, a takarmány felhasználhatóságáról az Állomás – a takarmánybiztonság szempontjainak figyelembevételével – az (1) bekezdésben foglalt tilalom bevezetését követő 30 napon belül dönt.
(3)29 A nemkívánatos anyagot a megengedettnél nagyobb mértékben tartalmazó takarmány esetén az Állomás meghatározza – a (4) bekezdésre is figyelemmel – a felhasználás módját, helyét, amellyel biztosítható, hogy a takarmány nemkívánatos anyag tartalma a megengedett mértéken belül maradjon. Amennyiben ez nem lehetséges, az Állomás elrendeli a takarmány megsemmisítését, a környezetvédelmi előírások figyelembevételével. Az ezekhez kapcsolódó szállítást az Állomás engedélyezi.
(4)30 A megengedettnél nagyobb mértékben nemkívánatos anyagot tartalmazó takarmányt tilos hígítási célból összekeverni ugyanolyan vagy más takarmánnyal.
(5) A felhasználás módjának betartását az Állomás a helyszínen köteles ellenőrizni.
16. § (1) Az állatok fehérjeellátásának javítására használható egyes termékek felhasználását és alkalmazási jegyzéküket a Takarmánykódex 4. számú mellékletének 16. fejezete tartalmazza.
(2) A különleges táplálási célokat szolgáló takarmányok felhasználásának szabályozását, valamint a kutyák és macskák különleges táplálási céljait szolgáló takarmányainak energiaérték számítását a Takarmánykódex 13. számú melléklete tartalmazza.
17. § (1)31 A takarmány etethetőségi/felhasználhatósági, illetve minőségmegőrzési idejének lejártakor (a továbbiakban: lejárt takarmány) a takarmány tulajdonosa vagy forgalomba hozója köteles a lejárt takarmánytételt az Állomásnak bejelenteni.
(2) A bejelentésnek tartalmaznia kell:
a) a bejelentő nevét és telephelyét,
b) a takarmány tárolási helyét,
c) a takarmány nevét és tömegét,
d) a takarmány előállítási idejét és helyét,
e)32 a takarmány etethetőségi/felhasználhatósági, illetve minőségmegőrzési idejének lejárati időpontját.
(3) A lejárt takarmány további forgalmazásához és felhasználásához az Állomás engedélye szükséges. Az Állomás intézkedéséig a lejárt takarmány tulajdonosának, importőrének, illetve felhasználójának biztosítania kell, hogy az ilyen takarmány forgalmazásra vagy felhasználásra ne kerüljön.
(4) A bejelentés kézhezvételétől számított 7 munkanapon belül a takarmányfelügyelő helyszíni szemlét tarthat. Az Állomás a rendelkezésére álló adatok, a helyszíni szemle tapasztalatai, illetve a szükséges vizsgálatok alapján dönt a bejelentés időpontjától számított 14 napon belül, illetve ha laboratóriumi vizsgálat is szükséges, 30 napon belül, a takarmány felhasználhatóságáról, értékcsökkentésének mértékéről.
18. §33 (1) A takarmány-adalékanyagok engedélyezésére, nyilvántartásba vételére és jelölésére a takarmányozási célra felhasznált adalékanyagokról szóló, 2003. szeptember 22-i 1831/2003/EK európai parlamenti és tanácsi rendelet (a továbbiakban: 1831/2003/EK rendelet) előírásait, valamint a Takarmánykódex 4. számú melléklete III. fejezetének 2. számú függelékében foglaltakat kell alkalmazni.
(2) Állatok fehérje ellátásának javítására használható termék engedélyezésére a Takarmánykódex 14. számú mellékletének I. fejezetét kell alkalmazni.
(3) Ha az engedélyezett takarmány-adalékanyag felhasználásával előállított takarmány etetése következtében az állatnál, illetve az állati eredetű terméket fogyasztó embernél új élettani hatások lépnek fel, a Mezőgazdasági Szakigazgatási Hivatal területi szerve ideiglenesen megtiltja a takarmány felhasználását és beszerzi a Mezőgazdasági Szakigazgatási Hivatal Központjának véleményét. A Mezőgazdasági Szakigazgatási Hivatal Központja a területi szervétől és a takarmány előállítójától beszerzett információk és a rendelkezésre álló szakmai dokumentumok, laboratóriumi vizsgálati eredmények, valamint a gyakorlati tapasztalatok alapján nyilvánít véleményt a kérdéses takarmány felhasználhatóságáról. A Mezőgazdasági Szakigazgatási Hivatal területi szerve ennek figyelembevételével megteszi a Tv. 14. §-a alapján a szükséges intézkedéseket.
(4) Az 1831/2003/EK rendelet 13. cikkének (1) bekezdése szerinti vélemény iránti kérelmet a nemzeti referens küldi meg az Európai Élelmiszer-biztonsági hatóságnak.
19. §34 (1)35 Kísérlet céljára a Tv. 8. §-a szerinti eseti jelleggel a Mezőgazdasági Szakigazgatási Hivatal Központja engedélyezheti a közösségi szinten nem engedélyezett adalékanyagok vagy állatok fehérje ellátásának javítására használható termékek felhasználását, ha a kísérleteket a Takarmánykódex 4. számú melléklete III. fejezetének 2. számú függelékével, valamint a Takarmánykódex 14. számú mellékletének I. fejezetével összhangban végzik.
(2)36 Adalékanyagok kísérleti céllal való engedélyezése esetén be kell tartani az 1831/2003/EK rendelet 3. cikkének (2) bekezdésében foglaltakat. A kísérlet céljára engedélyezett új takarmány forgalomba nem hozható. A kísérletbe bevont állatokból származó élelmiszerek felhasználásáról a hatósági állatorvos dönt a külön jogszabályban foglaltak szerint.
(3) Az (1) bekezdés szerinti új takarmány kísérleti célú előállítása és felhasználása csak a kísérleti engedélyben meghatározott
a) időpontig, de legfeljebb egy évig,
b) helye(ke)n, mennyiségben és minőségben,
c) előállítási, felhasználási és ellenőrzési feltételek betartásával
történhet.
(4) A kísérleti engedély egy alkalommal, legfeljebb egy évvel meghosszabbítható.
(5) Az OMMI a kísérleti engedély iránti kérelmet elutasítja, a már megadott kísérleti engedélyt visszavonja vagy az abban engedélyezett tevékenység végzését felfüggeszti, ha
a) a benyújtott dokumentáció nem felel meg a valóságnak,
b) az engedélyezési kérelemben leírt takarmányozás-élettani hatást a takarmány nem éri el,
c) a vizsgálati eredmények nem felelnek meg a garantált értékeknek,
d) a takarmány vizsgálata során a dokumentációban nem megjelölt, azonosíthatatlan, ismeretlen anyag jelenléte állapítható meg,
e) a toxikológiai, kihasználási, illetve az állatetetési kísérletek során káros élettani hatást mutat,
f) komponensei között, valamint más takarmány-alapanyagokkal, illetve más takarmány-adalékanyagokkal összeférhetetlenség mutatható ki.
(6) Az OMMI a kísérleti engedély iránti kérelmet akkor is elutasítja, ha
a) a termék vizsgálatára nincs hitelt érdemlő, pontos és megismételhető analitikai módszer,
b) a takarmány vizsgálata során megállapítható, hogy tiltott anyagot tartalmaz, illetve a nemkívánatos anyagok mennyisége meghaladja a jogszabályban előírt legmagasabb értéket.
(7) A kísérleti célra engedélyezett, a kísérleti engedély érvényességi ideje alatt fel nem használt takarmányt a környezetvédelmi előírások betartásával meg kell semmisíteni. Az Európai Unió tagállamain kívüli országból behozott takarmányt vissza kell szállítani abba az országba, ahonnan behozták, ha ez nem lehetséges, a takarmányt a környezetvédelmi előírások betartásával meg kell semmisíteni. A megsemmisítés, illetve a visszaszállítás költségei az engedélyest terhelik.
19/A. §37 (1) Azokat a takarmány-adalékanyagokat, illetve állatok fehérje ellátásának javítására használható bizonyos termékeket, amelyek a Takarmánykódex 4. számú mellékletében nincsenek felsorolva, de Magyarországon előállítási, forgalomba hozatali és felhasználási engedéllyel rendelkeznek, az engedélyesnek az OMMI részére 2004. március 20-ig be kell jelenteni.
(2) A bejelentésnek tartalmaznia kell a takarmány-adalékanyag, illetve az állatok fehérje ellátásának javítására használható bizonyos termék nevét, az előállítására jogosult(ak) körét, a termék összetételét, garantált beltartalmát, az engedély számát és keltét, valamint a termék felhasználásának körét és feltételeit.
(3) Az (1) bekezdésben felsorolt termékeket az OMMI jelenti be az Európai Bizottság részére.
(4) Az (1) bekezdésben felsorolt termékeket a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napjától – a kísérleti engedéllyel rendelkező termékeken kívül – tilos Magyarországon forgalomba hozni és felhasználni, kivéve, ha azok az Európai Unióban engedélyezésre kerültek.
(5) A (4) bekezdés szerinti engedély megszerzése érdekében a közösségi engedély megadásához szükséges dokumentációkat (Takarmánykódex 4., illetve 14. számú melléklete) magyar és angol nyelven kell benyújtani az OMMI-nél működő nemzeti referens részére. A nemzeti referens szükség esetén hiánypótlást kérhet. A nemzeti referens megküldi az engedély iránti kérelmet az Európai Bizottság részére. Az Európai Bizottság megállapításairól a nemzeti referens a kérelmezőt haladéktalanul értesíti.
(A Tv. 9. §-ához)
20. § (1) Takarmány csak zárt és új csomagolóeszközben, zárt tartályban vagy zárt helyiségben, illetve fedett módon ömlesztve szállítható, tárolható és hozható forgalomba. A szálas- és tömegtakarmányok ömlesztve, fedett módon szállíthatók, tárolhatók és hozhatók forgalomba.
(2) A csomagolóeszközt vagy tartályt úgy kell lezárni, hogy a felnyitással a zárás megsérüljön és azt eredeti formájában ne lehessen újra lezárni.
(3) Amennyiben a csomagolás megsérül, a benne lévő takarmány újracsomagolása kizárólag akkor lehetséges, ha annak azonossága, minősége és biztonsága változatlan maradt. Egyéb esetekben az újracsomagolás tilos. A csomagolóeszközt újrafelhasználni, visszaváltani, cserélni tilos. A csomagolóeszköz megsemmisítésénél a vonatkozó állategészségügyi és környezetvédelmi előírásokat be kell tartani.
(4) Állatgyógyászati készítményt tartalmazó takarmányt csak bontatlan csomagolásban vagy zárt tartályban lehet forgalomba hozni. Egyéb takarmányok esetében a bontott csomagoláson a takarmány eredeti jelölését biztosítani kell.
21. § (1) A csomagolóeszköz, tartály, tárolóhely, szállítóeszköz az állatok egészségére ártalmas anyagot nem tartalmazhat, és biztosítania kell a takarmány minőségének megóvását.
(2) A csomagolásnak védenie kell a takarmányt a szennyeződésektől, a táplálóanyag-tartalom csökkentő és a minőségrontó hatásoktól.
(3) Gyógyszeres takarmány, takarmány-adalékanyag vagy a 14. § (3) bekezdése és a 15. § (3) bekezdése szerinti takarmányok szállítása esetén a takarmányokat szállító tartálykocsit vagy konténert a kirakodást követően ki kell tisztítani, illetve a takarmányok szállítása után a raktér, illetve a konténer szennyeződéseit el kell távolítani.
(4) A létesítményekben tárolt takarmányokról nyilvántartást kell vezetni, amelyek tartalmazzák a takarmányok származási helyét, érkezésének idejét és mennyiségét, valamint a kiszállítás idejét és helyét.
22. §38 (1) A takarmány-alapanyagok csomagolóeszközén, címkéjén, illetve ömlesztve vagy tartályban való szállítás esetén a kísérő okmányon jól láthatóan, olvashatóan és eltávolíthatatlanul – a Magyarországon forgalomba hozatalra kerülő takarmányok esetén magyar nyelven – fel kell tüntetni a következő adatokat:
a) a szálas- és tömegtakarmányok kivételével a „takarmány-alapanyag” megnevezést,
b) a Takarmánykódex 1. számú melléklete szerinti adatokat, a következők figyelembevételével:
ba) a takarmány-alapanyag megnevezését a Takarmánykódex 1. számú melléklete szerint, és e melléklet IV. fejezetében felsorolt feldolgozási eljárások alkalmazása esetén a feldolgozásra általánosan használt nevet/jelzőt,
bb) a Takarmánykódex 1. számú mellékletének I. fejezetében felsorolt takarmány-alapanyagok esetén a Takarmánykódex 1. számú mellékletének I. fejezetében szereplő táblázatok 4. oszlopában feltüntetett beltartalmi értékeket, illetve az előállító által ezeken kívül garantált beltartalmi értéket,
bc) a Takarmánykódex 1. számú mellékletének I. fejezetében fel nem sorolt takarmány-alapanyagok esetén a Takarmánykódex 1. számú mellékletének II. fejezetében feltüntetett beltartalmi értékeket,
c) a takarmány nettó tömegét, szilárd halmazállapotú takarmány esetén nettó tömegegységben, folyékony halmazállapotú takarmány esetében nettó térfogat vagy tömegegységben kifejezve,
d) a takarmány-előállító üzem nevét vagy cégnevét és címét vagy székhelyét, valamint regisztrációs számát, illetve engedélyezési számát,
e) tételszámot vagy bármely más adatot, amely lehetővé teszi a takarmány-alapanyag nyomon követését a nyilvántartásba vett takarmány-előállító üzemnél,
f) annak a személynek a nevét vagy cégnevét, valamint címét vagy székhelyét, aki az e bekezdésben említett adatokért felelős, ha az nem azonos a d) pontban szereplő előállítóval.
(2) A takarmány-alapanyagok csomagolóeszközén, címkéjén, illetve ömlesztve vagy tartályban való szállítás esetén a kísérő okmányon az (1) bekezdésben foglaltakon kívül, azoktól elkülönítetten egyéb információk is feltüntethetők, amennyiben ezek az információk olyan objektív vagy mérhető értékekre, jellemzőkre vonatkoznak, amelyek igazolhatók, és nem tévesztik meg a vásárlót.
(3) A végső felhasználóknak szánt, 10 kg-ot meg nem haladó tömegű takarmány-alapanyagok esetében az (1) és a (2) bekezdésben meghatározott adatokról, információkról a forgalomba hozatal helyén is lehet tájékoztatni a vásárlót.
(4) Amennyiben a forgalmazás során valamely tételt megosztanak, az (1) bekezdés szerinti adatokat az eredeti tételre való utalással együtt újra fel kell tüntetni az adott tétel minden egyes újabb egységének csomagolóeszközén, címkéjén, illetve ömlesztve vagy tartályban való szállítás esetén a kísérő okmányon.
(5) Amennyiben a forgalomban lévő takarmány-alapanyag összetétele megváltozik, az (1) bekezdésben említett jellemzőket a változásnak megfelelően módosítani kell, az új jellemzőket feltüntető személy felelősségére.
22/A. §39 (1) A 22. §-tól eltérően a 22. § (1) bekezdésének bb) és bc) pontjában, valamint a Takarmánykódex 1. számú melléklete II. fejezete 3. pontjának második és harmadik franciabekezdésében említett adatok feltüntetése nem kötelező az alábbi esetekben:
a) amennyiben a vásárlás előtt a végső felhasználó írásban kijelenti, hogy nem tart igényt ezekre az információkra,
b) azon állati vagy növényi eredetű, friss vagy tartósított, esetleg egyszerű fizikai kezelésnek alávetett takarmány-alapanyagok forgalmazása esetében, amelyeket 10 kg-ot meg nem haladó tömegenként, kedvtelésből tartott állatok számára közvetlenül a végső felhasználó részére értékesít a Magyarországon bejegyzett eladó.
(2) A 22. §-tól eltérve
a) nem kell megkövetelni a 22. § (1) bekezdése szerinti adatok feltüntetését olyan Magyarországon gazdálkodó termelő által Magyarországon előállított növényi vagy állati eredetű, természetes állapotú, friss vagy tartósított, fizikai kezelésnek alávetett vagy anélkül forgalmazott, tartósítószerek kivételével adalékanyagot nem tartalmazó takarmány-alapanyag esetében, amelyet az előállító kínál eladásra Magyarországon való felhasználásra állattartónak,
b) nem kell megkövetelni a 22. § (1) bekezdésének b)–c) pontjában, valamint a Takarmánykódex 1. számú mellékletének II–IV. fejezete szerinti adatok, jellemzők feltüntetését olyan növényi vagy állati eredetű melléktermékek forgalmazása esetén, amelyek agráripari feldolgozásból származnak, és nedvességtartalmuk meghaladja az 50%-ot.
22/B. §40 (1) A Takarmánykódex 1. számú mellékletének I. fejezetében felsorolt takarmány-alapanyagok csak az ott meghatározott egyedi néven és azzal a feltétellel forgalmazhatóak, ha megfelelnek az ott megállapított leírásoknak.
(2) A Takarmánykódex 1. számú mellékletének I. fejezetében fel nem sorolt takarmány-alapanyagok is forgalmazhatóak, feltéve hogy ezek a takarmány-alapanyagok más néven, illetve más feltételekkel kerülnek forgalomba, mint a Takarmánykódex 1. számú mellékletének I. fejezetében felsorolt anyagok, úgy, hogy ezen takarmány-alapanyagok ne téveszthessék meg a vásárlókat a takarmány-alapanyag azonosságát illetően.
22/C. §41 A takarmány-adalékanyagok és a takarmány-adalékanyagokat tartalmazó előkeverékek jelölésére a takarmányozási célra felhasznált adalékanyagokról szóló, 2003. szeptember 22-i 1831/2003/EK európai parlamenti és tanácsi rendelet előírásait kell alkalmazni.
22/D. §42 A takarmány-adalékanyagok körébe nem tartozó állatok fehérje ellátásának javítására használható termékek, valamint az ezeket tartalmazó előkeverékek csomagolóeszközén, címkéjén, illetve ömlesztve vagy tartályban való szállítás esetén a kísérő okmányon a Takarmánykódex 14. számú mellékletének II. fejezetében felsorolt adatokat fel kell tüntetni.
22/E. §43 (1) A forgalomba hozott takarmánykeverékeket a Takarmánykódex 7. számú melléklete szerint kell jelölni.
(2) A különleges táplálási igényeket kielégítő takarmányok esetében az (1) bekezdésben foglaltakon kívül a Takarmánykódex 13. számú mellékletében foglalt jelölési előírásokat is alkalmazni kell.
(3) A baromfi takarmánykeverékek energia értékét a Takarmánykódex 5. számú melléklete szerint kell kiszámítani és jelölni.
23. § (1) A ,,csak takarmányozási célra'' felirat a címkén, illetve a takarmány kísérő okmányán csak akkor alkalmazandó, ha a takarmány összetéveszthető élelmiszerrel.
(2)44
(3) Vényköteles gyógyszert tartalmazó takarmány címkéjén, minőségi bizonyítványán jól olvashatóan fel kell tüntetni a ,,CSAK ÁLLATORVOSI VÉNYRE'' feliratot, valamint egy legalább 20 mm x 20 mm nagyságú kék keresztet.
24. § (1)45 A saját célra előállított takarmányok – az elsődleges előállítású takarmányok kivételével – csomagolóeszközén, címkéjén, illetve ömlesztve vagy tartályban való szállítása esetén a kísérő okmányon fel kell tüntetni a Takarmánykódex 7. számú melléklete I. fejezete 1. pontjának a), b), j) és m) alpontjában foglaltakat.
(2) Amennyiben a takarmány-előállító üzemben a saját célra történő előállításon kívül forgalomba hozatal céljára is történik takarmány-előállítás, úgy azokat a takarmányokat, amelyeket saját célra használnak fel ,,SAJÁT ÁLLATÁLLOMÁNY ETETÉSÉRE'' felirattal kell ellátni.
(3) A forgalomba hozatalra szánt szálas- és tömegtakarmányok csomagolóeszközén, címkéjén, illetve ömlesztve vagy tartályban való szállításnál a kísérő okmányon a Takarmánykódex 1. számú mellékletében meghatározott adaton kívül fel kell tüntetni a takarmány nevét, valamint előállításának helyét és évét.
(4)46 A géntechnológiával módosított takarmányok jelölésére alkalmazni kell az 1829/2003/EK rendelet előírásait is.
(5) A Magyarországon előállított, de exportra szánt takarmánynak meg kell felelnie a megrendelő, illetve a célország előírásainak.
25. § (1) A Minisztérium a hatósági ellenőrzések során vett takarmányminták vizsgálatára alkalmas laboratóriumokat az engedélyezett és akkreditált laboratóriumok közül jelöli ki. Nem kerülhet kijelölésre a takarmány-előállításban és forgalomba hozatalban érdekelt létesítmény laboratóriuma.
(2)47 A Minisztérium az Európai Unió takarmányozási bizottságainak munkájában részt vevő magyar tagokat és az új takarmányok engedélyezési és nyilvántartásba vételi eljárását irányító és összefogó nemzeti referenst a Magyar Takarmánykódex Bizottság javaslata alapján jelöli ki.
(3)48 A nemzeti referens részt vesz a takarmány-adalékanyagok és állatok fehérje ellátásának javítására használható termékek engedélyezésére vonatkozó jogszabályok szakmai előkészítésében, véleményezi a takarmány-adalékanyagok és az állatok fehérje ellátásának javítására használható termékek közösségi engedélyezési eljárásában a szakmai dokumentumokat, és szükség esetén javaslatot tesz a kiegészítések és módosítások megtételére. A nemzeti referens tevékenysége során együttműködik a Magyar Takarmánykódex Bizottsággal és a nemzeti referencia laboratóriummal.
(4) A Minisztérium költségvetéséből biztosítja az OMMI, az ÁOGYTI és az Állomás azon hatósági feladatainak költségeit, amelyekhez díjtétel nem kapcsolódik, illetve az OMMI és az ÁOGYTI által működtetendő információs rendszer kialakításának és működtetésének költségeit.
(5)49 A Minisztérium megküldi az Európai Unió Bizottságának:
a) a takarmányozási hatóságok nevét, címét, illetékességi területét,
b) az (1) bekezdés szerint kijelölt laboratóriumok jegyzékét, a vizsgálatok körének feltüntetésével,
c) minden év április 1-jéig a hatósági ellenőrzések tapasztalatairól szóló éves jelentést.
26. § Az OMMI
a) évente közzéteszi a Minisztérium hivatalos lapjában a takarmányvizsgálati engedéllyel rendelkező laboratóriumok jegyzékét és az azokban engedélyezett vizsgálatok körét,
b) részt vesz a Magyar Szabványügyi Testület takarmányvizsgálati módszerekre vonatkozó szabványosítási munkájában, véleményezi a laboratóriumi vizsgálatok nemzetközi szabvány-tervezeteit,
c) a hazai elterjesztése érdekében javaslatot tesz az átvett nemzetközi vizsgálati módszereknek a Takarmánykódex 3. kötetében való megjelentetésére,
d) elvégzi az új vizsgálati módszerek érvényesítését,
e) térítés ellenében módszertani tanfolyamokat szervez,
f) működteti az állatállomány takarmányellátását szolgáló hazai előállítású és importált takarmányok mennyiségére vonatkozó információs rendszert a hivatalos statisztikai adatoknak, a Minisztérium adatainak, valamint az ÁOGYTI létesítményekre vonatkozó adatainak a felhasználásával, melynek eredményeiről a Minisztériumot folyamatosan tájékoztatja,
g) a Minisztérium által készített éves jelentés elkészítésében közreműködik az új takarmányok és a takarmányvizsgáló laboratóriumok engedélyezése, a takarmányvizsgáló laboratóriumok ellenőrzése, a takarmányok mennyiségi adatai tekintetében.
27. § (1) Az engedélyköteles takarmányvizsgáló laboratóriumokat érzékszervi, fizikai, kémiai-mikrobiológiai vizsgálatokra vonatkozóan az OMMI minősíti, nyilvántartja és – a Tv. 11. §-a (3) bekezdésének g) pontja kivételével – ellenőrzi.
(2) Az engedély megszerzésére nem kötelezett takarmányvizsgáló laboratóriumokat az OMMI nyilvántartja. A laboratóriumnak a nyilvántartáshoz minden év január végéig meg kell küldenie az OMMI-nek a (3) bekezdés a), b), e)–g) pontja szerinti adatokat.
(3) Az engedélyköteles takarmányvizsgáló laboratóriumnak a minősítés és engedélyezés iránti kérelmét két példányban az OMMI-hez kell benyújtania. A kérelemnek tartalmaznia kell:
a) a laboratórium nevét, címét, telephelyét, illetve telephelyeit,
b) a laboratórium vezetőjének nevét, szakképzettségét,
c) a takarmányvizsgálaton kívüli egyéb tevékenységi kör megjelölését,
d) a laboratórium helyszínrajzát,
e) a takarmányvizsgálati kör megnevezését, a vizsgálati módszerek megjelölésével,
f) a vizsgálatok műszaki, technikai és személyi feltételeit,
g) a laboratóriumi nyilvántartás és adatszolgáltatás rendszerét.
(4) Az OMMI a kérelem kézhezvételét követően helyszíni szemlét tart, valamint összehasonlító vizsgálatokat kezdeményez.
(5) Az OMMI a minősítő eljárás eredményei alapján javaslatot tesz a Minisztérium részére az engedélyezhető vizsgálatok körére és módszereire, a Minisztérium ez alapján dönt az engedély megadásáról. A Minisztérium által kiadott engedély a visszavonásig érvényes.
(6) Az OMMI nem javasolja az engedély megadását, ha
a) a helyszíni szemle alapján megállapítja, hogy a takarmányok más termékcsoporttól elkülönített fogadása, előkészítése, kezelése nem biztosítható,
b) a technikai, műszaki, illetve személyi feltételek elégtelenek a vizsgálatok elvégzéséhez,
c) az összehasonlító vizsgálat eredményeinek eltérése a 15. számú mellékletben előírt megengedhető eltéréseknél nagyobbak,
d) az ÁOGYTI-től megkért szakvélemény az állatgyógyászati hatóanyag vizsgálat engedélyezését nem javasolja.
(7) Az engedélyköteles laboratórium köteles az OMMI-nak bejelenteni a (2) bekezdés a)–c) és e)–g) pontjaiban történt változásokat, azok megvalósulásától számított 8 napon belül.
(8) Az OMMI nyilvántartást vezet a takarmányvizsgálati engedéllyel rendelkező laboratóriumokról, a vizsgálati tevékenységekről, illetve az engedélyek érvényességéről.
(9) Magyarországon a takarmányvizsgálatok területén a referencia laboratórium az OMMI Központi Laboratóriuma.
28. § (1) Az OMMI a takarmányvizsgáló laboratóriumok ellenőrzése során évente legalább egyszer
a) az engedélyköteles takarmányvizsgáló laboratóriumoknál laboratóriumok közötti összehasonlításokat és körvizsgálatokat végez,
b) az engedély megszerzésére nem kötelezett takarmányvizsgáló laboratóriumoknál, beleértve a takarmányelőállító üzemek laboratóriumait is, körvizsgálatokat végez.
(2) Az OMMI ellenőrzi valamennyi takarmányvizsgáló laboratórium jártassági körvizsgálatokon való részvételét.
(3) Az OMMI a laboratóriumok helyszíni szemléje során ellenőrzi:
a) a minősítési dokumentációban, valamint a nyilvántartásokban foglalt adatok megfelelőségét,
b) az engedélyben szereplő vizsgálatok tekintetében a környezeti, műszaki és személyi feltételek meglétét,
c) az engedélyezett vizsgálatoknak a 15. számú melléklet szerinti megfelelőségét.
29. §50
30. § Az OMMI-nek a Tv. 11. §-ának (2) bekezdésében és 14. §-ának (1) bekezdésében foglalt feladatainak ellátása érdekében az OMMI hatósági feladatokkal megbízott munkatársa beléphet a létesítmények és laboratóriumok területére, a létesítményre, a laboratóriumra, a takarmányokra, a vizsgálatokra vonatkozó nyilvántartásokat, dokumentációt megtekintheti, és azokról – az üzemi, illetve üzleti titok védelmére vonatkozó szabályok betartásával – másolatot készíthet, és az engedélyezési eljárás alatt álló új takarmányból térítésmentesen mintákat vehet.
31. § (1) Az ÁOGYTI a megyei takarmányfelügyelők ellenőrző tevékenységének szakmai irányítási tevékenysége keretében
a) meghatározza az egységes ellenőrzés rendjét és módját,
b) a szakmai feladatokat összehangolja és végrehajtásukat ellenőrzi,
c) biztosítja a nagy fontosságú és veszélyes, import és hazai előállítású takarmány-alapanyagok, -adalékanyagok és előkeverékek ellenőrzésének koordinálását,
d) kialakítja és működteti az import takarmányok követhetőségének, ellenőrzésének és mintavételezésének rendszerét, valamint összehangolja a szükséges hatósági intézkedéseket.
(2) Az ÁOGYTI a takarmányfelügyelők által vett hatósági minták laboratóriumi vizsgálati eredményeinek ismeretében és a területi ellenőrzési tapasztalatok értékelése alapján:
a) szakmailag irányítja és koordinálja az egyes minőséghibák megszüntetésére, illetve a takarmányok biztonságos felhasználását veszélyeztető nemkívánatos és tiltott anyagot, mikrobiológiai szennyezettséget tartalmazó takarmányok felhasználásának tilalmára, illetve korlátozására vonatkozó intézkedéseket,
b) az Állomásoktól kapott információk és a saját tapasztalatai alapján folyamatosan tájékoztatja a Minisztériumot a takarmányok minőségéről és biztonságáról, valamint a takarmányok előállításáról, tárolásáról, exportjáról, importjáról az országon való átszállításáról, forgalomba hozataláról és a létesítmények ellenőrzési tapasztalatairól,
c) az állatgyógyászati készítmények vonatkozásában a gyógyszeres takarmányokat vizsgáló laboratóriumokat évente legalább egy alkalommal ellenőrzi,
d) az Állomások bevonásával elkészíti az ellenőrzés, mintavétel és vizsgálatok országos éves tervét – az előállított, forgalomba hozott takarmányok mennyiségének és féleségének, valamint a minőségi hibák előfordulásának és a takarmánybiztonsági követelményeknek a figyelembevételével –, amelyet a Minisztérium hagy jóvá,
e) a Minisztérium által készített éves jelentés elkészítésében közreműködik a takarmány-előállítás, tárolás, import, export és takarmányforgalmazás hatósági ellenőrzésének tapasztalatai, a vett minták vizsgálati eredményeinek értékelése alapján a takarmányok minőségének és biztonságának helyzete és a létesítmények engedélyezése tekintetében,
f) javaslatot tesz a Minisztérium által engedélyezésre kerülő mintavételi eszközökre és azok alkalmazására.
(3)51 Az ÁOGYTI intézkedési tervet készít arra az esetre, ha a takarmány-ellenőrzés a takarmányról megállapítja, hogy az emberi, állati egészségre vagy a környezetre komoly kockázatot jelent. Az intézkedési terv a jogszabályokkal összhangban meghatározza az alkalmazandó intézkedések körét, az érintett hatóságok feladatait, felelősségét és az információtovábbítás módjait. Az ÁOGYTI által elkészített tervet a Minisztérium hagyja jóvá. A programot folyamatosan felül kell vizsgálni.
32. § Az Állomások a Tv. 11. §-ának (4) bekezdésében leírt feladataik végrehajtásával kapcsolatos tapasztalataikról és a megtett intézkedéseikről éves jelentést készítenek. A jelentést az ÁOGYTI-nek kell megküldeni.
33. § (1) A takarmányfelügyelő ellenőrzi:
a) a takarmány-előállító üzemekben a forgalmazási célból előállított takarmányok esetében:
1. a raktárakat, a raktározott takarmányok minőségének megóvását, kezelését, elkülönítését,
2. a takarmányok minőségét és biztonságos felhasználását befolyásoló technológiai berendezések rendeltetésszerű használatát,
3. a takarmányok fizikai, kémiai és érzékszervi tulajdonságait,
4.52 a takarmányok kiszerelését, etethetőségi/felhasználhatósági, illetve minőségmegőrzési idejét,
5. az üzem minőségbiztosításának hatékonyságát,
6. a takarmány-alapanyagokra, az előállításra, a végtermékre, valamint a tárolásra és szállításra vonatkozó nyilvántartásokat és dokumentációkat,
7. a takarmányok összetételét, beltartalmát,
8. a nemkívánatos és tiltott anyag tartalmat, a takarmányba kevert állatgyógyászati készítmények hatóanyag-tartalmát, a takarmány mikrobiológiai állapotát, kártevő mentességét,
9. a takarmány-adalékanyagok felhasználását,
10. a működési engedélyben foglaltak betartását,
11. a takarmány jelölését,
b) a takarmány-előállító üzemekben a saját célra előállított takarmányok esetében az a) pont 1., 2., 6., 8–11. alpontjában foglaltakat,
c) a takarmány-előállító üzemen kívül előállított takarmányoknál, szükség esetén a mezőgazdasági termelés helyszínén:
1. forgalomba hozatal esetén a takarmány minőségének megóvását, a kártevőktől, a nemkívánatos és tiltott anyagoktól való mentességet, a mikrobiológiai állapotot és a jelöléseket,
2. a saját célra történő felhasználás esetén a kártevőktől, a nemkívánatos és tiltott anyagoktól való mentességet, a mikrobiológiai állapotot és a jelöléseket,
d) a takarmány tároló, forgalmazó és a felhasználó helyen az ott tárolt takarmányok
1. minőségének megóvását, elkülönítését, kezelését,
2. mennyiségéről, minőségéről és értékesítéséről szóló nyilvántartásokat,
3.53 csomagolását, jelölését, etethetőségi/felhasználhatósági, illetve minőségmegőrzési idejét,
4. érzékszervi, fizikai tulajdonságait,
5. összetételét, beltartalmát, a nemkívánatos és tiltott anyag tartalmát, a takarmányba kevert állatgyógyászati készítmények hatóanyag-tartalmát, mikrobiológiai állapotát, kártevő mentességét,
6. működési engedélyben foglaltak betartását,
e) a közvetítők esetében a működési engedély meglétét, a közvetítő tevékenységi körébe tartozó takarmányokról vezetett nyilvántartásokat,
f) a létesítmények rendjét, tisztaságát,
g) a takarmányok exportját, tranzitját és importját, a Takarmánykódex 12. számú melléklete szerint,
h) a takarmány-előállítás, tárolás, export, import, az országon történő átszállítás, forgalomba hozatal, szállítás során a takarmányok nyomon követhetőségét, a kritikus pontok figyelembevételével.
(2) A takarmányfelügyelő az ellenőrzés során a Takarmánykódex 11. számú mellékletében foglalt mintavételi szabályok szerint térítésmentesen mintát vehet, amelyről minden esetben mintavételi jegyzőkönyvet állít ki. A takarmányfelügyelő a Tv. 13. §-ának (2) bekezdése szerint vesz ellenmintát. Az ellenmintát az ellenminta vételét kérőnek kell tárolnia, a Takarmánykódex 11. számú mellékletében foglalt előírások szerint. Az ellenőrzés során a takarmányfelügyelő a mintavételeket a Minisztérium által jóváhagyott éves terv alapján végzi.
(3) A (2) bekezdés szerinti jegyzőkönyvnek tartalmaznia kell a megmintázott takarmány nevét, mennyiségét, termékszámát, tételszámát, az előállítás idejét, helyét, a takarmány nagykereskedelmi egységárát, a takarmány-előállító üzem, illetve forgalmazó hely nevét, a vizsgálatok megjelölését, valamint a mintavevő nevét és a takarmány-előállító üzemet, illetve forgalmazó helyet a mintavétel során képviselő nevét. A jegyzőkönyvben fel kell tüntetni az ellenminta vételét is.
(4) A hatósági mintavétel során vett takarmányminták vizsgálatainál a Takarmánykódex 10. számú mellékletében foglalt vizsgálati módszereket alkalmaznia kell minden e vizsgálatokra kijelölt laboratóriumnak.
(5) A takarmányfelügyelő által vett, a vizsgált tétellel azonos takarmányminták vizsgálatait a Minisztérium által kijelölt laboratóriumok végzik.
(6) A takarmányfelügyelő az ellenőrzésekről minden esetben jegyzőkönyvet vesz fel, amelyben rögzíteni kell az ellenőrzés során tapasztaltakat és a hozott intézkedéseket.
(7) A takarmányfelügyelő a takarmány-ellenőrzés céljából munkaidő alatt a munkaterületre bármikor beléphet. Az ellenőrzött köteles az ellenőrzést elősegíteni és a takarmányfelügyelő részére a szükséges adatokat, dokumentumokat, nyilvántartásokat és az ellenőrzés egyéb feltételeit biztosítani. A takarmányfelügyelő az ellenőrzés időpontjáról és köréről az ellenőrzöttet előzetesen nem értesíti.
34. § (1) Az ellenőrzés során, a felhasználás előtt az Állomásnak vizsgálat céljából mintát kell vennie abból a takarmány-alapanyagból, -adalékanyagból és előkeverékből, amelynek jelölései olyan mértékben hiányosak, hogy azok nem biztosítják a takarmány azonosítását, szakszerű és biztonságos felhasználását. A vett minták vizsgálatát az OMMI végzi. A vizsgálati eredmények, valamint a rendelkezésre álló dokumentumok alapján az Állomás dönt a takarmány-alapanyag, -adalékanyag és előkeverék felhasználhatóságáról.
(2) Az (1) bekezdésben foglalt vizsgálatok díjkötelesek, a díjak az OMMI bevételét képezik.
35. § Az OMMI, az ÁOGYTI hatósági feladatokkal megbízott munkatársa, valamint a takarmányfelügyelő hatósági igazolványának mintáját a 16. számú melléklet tartalmazza.
(A Tv. 14. §-ához)
36. §54
37. § (1) Az OMMI a takarmányvizsgáló laboratórium működési engedélyének módosítását javasolhatja a Minisztériumnak, ha
a) a dokumentációban, illetve a nyilvántartásokban foglalt adatok megváltoznak,
b) a bejelentett környezeti, műszaki és személyi feltételek megváltozása esetén kezdeményezett új összehasonlító vizsgálatok eredménye indokolja,
c) a helyszíni szemlék összehasonlító vizsgálatai, valamint a jártassági körvizsgálatok eredményei indokolják.
(2) Az OMMI a takarmányvizsgáló laboratórium működési engedélyének felfüggesztését javasolja a Minisztériumnak a visszavonásra alapot adó tények kivizsgálása idejére.
(3) Az OMMI a takarmányvizsgáló laboratórium működési engedélyének visszavonását javasolja a Minisztériumnak, ha
a) a laboratórium takarmányvizsgálati tevékenységét megszünteti,
b) a laboratórium nem vesz részt a jártassági körvizsgálaton, illetve megtagadja a helyszíni ellenőrzés lehetőségét,
c) a laboratórium a jártassági körvizsgálat, illetve annak egyszeri javító vizsgálata során a vizsgálatok több mint 70%-ára vonatkozóan nem felel meg,
d) a helyszíni ellenőrzések során tapasztaltak alapján megállapítható, hogy a laboratórium technikai, műszaki és személyi feltételei alkalmatlanok az engedélyben foglalt vizsgálatok elvégzésére.
(4) Az engedély megszerzésére nem kötelezett takarmányvizsgáló laboratóriumoknál, ha a vizsgálatok eredményei azt indokolják, a laboratóriumot az OMMI írásban felszólítja a tapasztalt vizsgálati hibák, hiányosságok megszüntetésére.
(5) A hatósági mintákat vizsgáló laboratóriumok esetében e minták vizsgálati jogosultsága visszavonható, ha azokat nem a Takarmánykódex 10. számú mellékletében előírt módszer szerint, illetve e rendelet 15. számú mellékletében foglaltaktól eltérően végzik. A visszavonást az ÁOGYTI vagy az Állomás kezdeményezésére az OMMI javasolja.
38. § (1)55 Az Állomás a takarmány-előállító üzem működési engedélyét felfüggesztheti, ha az ellenőrzés a működési engedélyben foglaltaktól eltérést állapít meg, az előállított takarmányok rossz minőségűek vagy veszélyeztetik az állatok, illetve az állati terméket fogyasztó emberek egészségét, továbbá, ha a takarmány-előállító üzem a 4. számú melléklet szerinti nyilvántartásokat nem, vagy nem megfelelően vezeti. Egy üzemben előállított takarmányok akkor tekinthetők rossz minőségűeknek, ha az azokból 6 hónap alatt vett, minimum 10 hatósági minta 60%-a a vizsgálatok értékelése során bármilyen okból kifogásolt, értékcsökkentett vagy bírságolt.
(2) A takarmány-előállító üzemek működési engedélye módosítható, ha
a) az engedéllyel rendelkező azt kéri,
b) az ellenőrzés megállapításai azt indokolják.
(3) A takarmány-előállító üzem működési engedélyét az Állomás visszavonja, ha
a) a felfüggesztés időtartama alatt a hatóság részéről megjelölt engedélytől való eltéréseket a takarmány-előállító üzem nem szüntette meg,
b) az Állomás az engedélyben foglaltaktól olyan jellegű eltérést állapít meg, amely által a takarmány folyamatosan veszélyezteti az állatok egészségét, illetve a takarmány-előállító üzem alkalmatlanná vált jó minőségű takarmány előállítására,
c)56 a 11. § (6) bekezdésében foglalt eset következik be.
(4) Az Állomás a takarmányt etetésre alkalmatlannak nyilvánítja, ha
a) a takarmány tiltott anyagot tartalmaz,
b)57 a megengedettnél nagyobb mértékben nemkívánatos anyagot tartalmaz, és ez a 15. § (3) bekezdésében foglaltak alapján nem szüntethető meg,
c) a takarmány mikrobiológiai állapota azt szükségessé teszi,
d) a takarmány egymással összeférhetetlen állatgyógyászati készítményeket tartalmaz,
e) a takarmánytételnek az előállítási hibából eredő keveredése, összetevő hiánya vagy többlete az ellenőrzés mellett végrehajtott kezeléssel, újbóli előállítással vagy takarmánybiztonsági problémát nem okozó más állatfajjal vagy korcsoporttal történő etetéssel nem szüntethető meg.
39. § (1) Az Állomás a takarmány-előállítást, tárolást, forgalmazást, felhasználást, szállítást, exportot, importot és az illetékességi területen való átszállítást felfüggeszti, ha
a) a takarmány olyan anyagot tartalmaz, amely közvetlenül az állat, közvetve az ember egészségét, illetve a környezetet veszélyeztetheti, károsíthatja, a takarmány rendeltetésszerű felhasználását akadályozhatja vagy ezek gyanúja áll fenn,
b) a takarmány jelölése vagy kísérő okmánya hiányos vagy hiányzik, illetve az nem ad megfelelő, egyértelmű tájékoztatást a termék nevére, származására, összetételére, beltartalmára, felhasználására,
c) az eredeti csomagolás megsérült,
d) a takarmány-ellenőrzés a Takarmánykódex 8. és 9. számú mellékletében foglalt előírásoktól való eltérést állapít meg,
e)58 a takarmány-előállító üzem a 33. § szerinti ellenőrzés során nem tesz eleget a 33. § (7) bekezdésében foglalt kötelezettségének, illetve az ellenőrzést bármely módon akadályozza.
(2) Az Állomás vizsgálatok alapján meghatározhatja azokat a feltételeket és időpontot, amelyekkel az (1) bekezdésben felsoroltak megszüntethetők, illetve amelyik időpontra a feltételeket meg kell valósítani. A feltételek biztosítása és az időpont betartása a takarmány tulajdonosának, illetve az importőrének a kötelessége.
(3) Az Állomás megtiltja a takarmány előállítását, tárolását, forgalmazását, felhasználását, exportját, importját, szállítását, ha az előírt feltételek a megadott határidőre nem teljesülnek.
(4) Az Állomás a takarmánytétel etetésre alkalmatlannak nyilvánítása esetén elrendelheti a takarmány megsemmisítését a környezetvédelmi előírások figyelembevételével. A megsemmisítésről a takarmány tulajdonosának, illetve importőrének kell gondoskodnia.
(5) Az Állomás kötelezi a takarmány-előállító üzemet a minőség-ellenőrzési szabályzat módosítására, az ezzel kapcsolatos vizsgálatok végzésére és a minőséghiba megszüntetésére, ha az ellenőrzés ismétlődő, vagy olyan minőséghibát tárt fel, amelynek a megszüntetésére a takarmány-előállító üzem elfogadott minőség-ellenőrzési szabályzata nem ad megfelelő megoldást.
(6) Az Állomás az ismeretlen dokumentációjú takarmány-alapanyagok és -adalékanyagok felhasználását megtilthatja.
(7) Zárlati károsító vagy Magyarországon nem honos károsító azonosítása vagy előfordulásának gyanúja esetén az Állomás értesíti az illetékes megyei növény- és talajvédelmi szolgálatot.
40. § (1)59 Az Állomás az etethetőségi/felhasználhatósági, illetve minőségmegőrzési időn túl tárolt takarmányok megsemmisítését laboratóriumi vizsgálat nélkül is elrendelheti, ha a takarmányfelügyelő a helyszíni szemle során megállapítja, hogy a takarmányban olyan helyrehozhatatlan károsodás keletkezett, amelynek következtében az takarmányozási célra nem használható fel.
(2) Szükség esetén a további felhasználhatóság, illetve a minőség romlásának megállapítására laboratóriumi vizsgálatot kell elrendelni. A szükséges vizsgálatok körét a takarmányfelügyelő állapítja meg. A vizsgálatnak ki kell terjednie mindazon kémiai, fizikai, érzékszervi, mikrobiológiai jellemzőkre, melyekben a takarmány az idő függvényében károsodhatott. E vizsgálatok díjkötelesek, amelyet annak kell megtérítenie, akinél a takarmányt vizsgálat alá vonták.
(3)60 Az Állomás az etethetőségi/felhasználhatósági, illetve minőségmegőrzési időn túl tárolt és minőséghibás takarmányok további felhasználása tekintetében az ÁOGYTI, illetve az OMMI szakvéleményét kérheti.
(4) A vizsgálati eredmények alapján az Állomás határozatban elrendelheti a takarmány
a)61 etethetőségi/felhasználhatósági, illetve minőségmegőrzési idejének meghatározott ideig történő meghosszabbítását, legfeljebb egy alkalommal,
b) felhasználásának, forgalmazásának, illetve további feldolgozásának korlátozását, más állatfajjal, illetve hasznosítási és korcsoporttal történő, meghatározott időn belüli feletetését,
ha kizárt az állat, illetve az állati eredetű élelmiszert fogyasztó ember egészségkárosításának lehetősége.
(5) Az elrendelt intézkedések végrehajtása annak a kötelessége, akinél a takarmányt vizsgálat alá vonták.
(6) A tiltott anyagot tartalmazó takarmány megsemmisítése az Állomás határozata alapján annak a kötelessége, akinél a takarmányt vizsgálat alá vonták. A megsemmisítésről jegyzőkönyvet kell felvenni.
41. §62 Az Állomásnak bejelentett takarmányokra vonatkozó vásárlói, illetve felhasználói panaszok kivizsgálása során, a bejelentő kérésére az etethetőségi/felhasználhatósági, illetve minőségmegőrzési időn belül, az előállító által meghatározott feltételek mellett tárolt takarmányból vett minták vizsgálatának díját
a) ha a takarmány azonosítható
1. a takarmány-előállító üzem fizeti, ha a vizsgálatok minőséghibát mutatnak ki,
2. a vizsgálatot kérő fizeti, ha a vizsgálatok minőséghibát nem mutatnak ki,
b) ha a takarmány azonosíthatatlan, a bejelentő fizeti.
42–44. §63
45. § (1) Ez a rendelet – a (2) bekezdésben foglalt kivétellel – a kihirdetését követő második hónap első napján lép hatályba.
(2) A 11. § (4)–(6) bekezdése, a 22. § (1) bekezdésének h) pontja, valamint a 38. § (3) bekezdésének c) pontja 2003. október 1-jén, a 7. § (5) és (6) bekezdése, a 25. § (2), (3) és (5) bekezdése és a 31. § (3) bekezdése pedig a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lép hatályba.
(3)64
(4)65 A 12. § (2) bekezdése, a 36. §, valamint a 6–13. számú melléklet a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján hatályát veszti.
(5)66
(6) E rendelet hatálybalépése előtt gyártott, a gyártás idején hatályos jogszabályi előírásoknak megfelelő takarmányok minőségmegőrzési idejük lejártáig hozhatók forgalomba, illetve használhatók fel.
(7)67
46. §68 (1) Ez a rendelet a takarmányok előállításáról, forgalomba hozataláról és felhasználásáról szóló 2001. évi CXIX. törvénnyel és a Magyar Takarmánykódex kötelező előírásairól szóló FVM rendelettel együtt a következő uniós jogi aktusoknak való megfelelést szolgálja:
a) a Tanács 79/373/EGK irányelve (1979. április 2.) a takarmánykeverékek értékesítéséről, valamint az azt módosító, a Tanács 86/354/EGK, 90/44/EGK, 90/654/EGK, 93/74/EGK, 96/24/EK irányelve, az Európai Parlament és a Tanács 2000/16/EK irányelve, a Bizottság 97/47/EK, 98/87/EK, 1999/61/EK irányelve,
b) a Tanács 95/53/EK irányelve (1995. október 25.) a takarmányok hivatalos ellenőrzésének szervezési alapelveiről, valamint az ezt módosító, a Tanács 1999/20/EK irányelve, az Európai Parlament és a Tanács 2000/77/EK, 2001/46/EK irányelve,
c) a Tanács 95/69/EK irányelve (1995. december 22.) a takarmányozási ágazatban működő létesítmények és forgalmazók engedélyezésének és nyilvántartásba vételének feltételeiről és az ezekkel kapcsolatos intézkedésekről, a 70/524/EGK, a 74/63/EGK, a 79/373/EGK és a 82/471/EGK irányelvek módosításáról, valamint az ezt módosító, a Tanács 1999/20/EK irányelve,
d) a Tanács 96/25/EK irányelve (1996. április 29.) a takarmány-alapanyagok forgalmáról, a 70/524/EGK, a 74/63/EGK, a 82/471/EGK és a 93/74/EGK irányelv módosításáról, valamint a 77/101/EGK irányelv hatályon kívül helyezéséről, valamint az azt módosító, a Bizottság 98/67/EK irányelve, a Tanács 1999/61/EK irányelve, az Európai Parlament és a Tanács 2000/16/EK és 2001/46/EK irányelve,
e) a Bizottság 2001/9/EK határozata (2000. december 29.) a 2000/766/EK tanácsi irányelv végrehajtásához szükséges ellenőrző intézkedésekről a szivacsos agyvelőgyulladás elleni védőintézkedés és az állati fehérje felhasználás területén, valamint az azt módosító, a Bizottság 2001/165/EK és 2002/248/EK határozata,
f) az Európai Parlament és a Tanács 2002/2/EK irányelve (2002. január 28.) az összetett takarmány forgalmazásáról szóló 79/373/EGK tanácsi irányelv módosításáról és a 91/357/EGK bizottsági irányelv hatályon kívül helyezéséről.
(2) Ez a rendelet a következő közösségi rendeletek végrehajtásához szükséges rendelkezéseket állapítja meg:
a) az Európai Parlament és a Tanács 1831/2003/EK rendelete (2003. szeptember 22.) a takarmányozási célra felhasznált adalékanyagokról,
b) az Európai Parlament és a Tanács 183/2005/EK rendelete (2005. január 12.) a takarmányhigiénia követelményeinek meghatározásáról.
1. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez69
2. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez70
szükséges vizsgálatok
|
|
100 x S |
|
CV % = |
––––––––– |
|
|
– |
|
|
x |
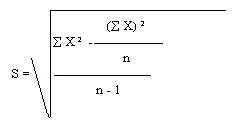
|
Takarmánycsoportok |
A mintában vizsgálandó |
CV % |
|---|---|---|
|
|
|
|
|
Vitamin mikroelem és egységes premix |
Vitaminok, illetve mikroelemek vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz max. |
5% |
|
Komplett premixek, adalékanyagok |
Nyomelemek, makroelemek, vagy más garantált alkotóanyag vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz max. 4 hatóanyag |
8% |
|
|
|
|
|
Koncentrátum, kiegészítő takarmányok |
Nyomelemek, makroelemek, vagy más garantált alkotóanyag vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz max. 4 hatóanyag |
10% |
|
|
|
|
|
A 2001. évi CXIX. törvény |
Nyomelemek, makroelemek, vagy más garantált alkotóanyag vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz |
12% |
3. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez71
4. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez72
|
Felhasználandó összetevők megnevezése |
Felhasználandó összetevők tételszámai/ |
Összetevők bemérendő mennyiségei kg |
Ténylegesen bemért mennyiségek kg |
Eltérés |
Bemérő aláírása |
|---|---|---|---|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ÖSSZESEN: |
|
|
|
|
|
|
Mosatási |
Eljárást |
Eljárást követően |
Mosató |
Mosató anyag felhasználása |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
|
sorszáma |
időpontja |
megnevezése, |
kritikus anyaga |
megnevezése, |
megnevezése |
mennyisége |
milyen |
takarmány tételszáma |
mosatóanyag felhasznált mennyisége |
időpontja |
maradék |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez
kereskedő aláírása)
6–13. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez73
14. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez74
Takarmány neve |
Beltartalmi értékek |
Állatfajok |
|||
|---|---|---|---|---|---|
A jelölés kötelező |
A jelölés fakultatív |
||||
1. |
2. |
3. |
4. |
||
Teljes értékű takarmányok |
Nyersfehérje |
Állatok, kivéve – a macska és a kutya kivételével – a kedvtelésből tartott állatokat |
A kedvtelésből tartott állatok, kivéve a macskát és a kutyát |
||
|
Lizin |
Sertés |
Állatok, a sertést kivéve |
||
|
Metionin |
Baromfi |
Állatok, a baromfit kivéve |
||
|
Cisztin |
|
Minden állat |
||
|
Treonin |
|
Minden állat |
||
|
Triptofán |
|
Minden állat |
||
|
Energiaérték |
|
Baromfi |
||
|
Keményítő |
|
Minden állat |
||
|
Összes cukor, szacharózban kifejezve |
|
Minden állat |
||
|
Összes cukor + keményítő |
|
Minden állat |
||
|
Kálcium |
|
Minden állat |
||
|
Nátrium |
|
Minden állat |
||
|
Magnézium |
|
Minden állat |
||
|
Kálium |
|
Minden állat |
||
|
Foszfor |
Halak a díszhalak kivételével |
Állatok, a halak kivételével |
||
Kiegészítő takarmányok – ásványi takarmányok |
|
|
|
||
|
Nyersrost |
|
Minden állat |
||
|
Nyers hamu |
|
Minden állat |
||
|
Nyersolajok és zsírok |
|
Minden állat |
||
|
Lizin |
|
Minden állat |
||
|
Metionin |
|
Minden állat |
||
|
Cisztin |
|
Minden állat |
||
|
Treonin |
|
Minden állat |
||
|
Triptofán |
|
Minden állat |
||
|
Kálcium |
Minden állat |
|
||
|
Foszfor |
Minden állat |
|
||
|
Nátrium |
Minden állat |
|
||
|
Magnézium |
Kérődzők |
Állatok, a kérődzőket |
||
|
Kálium |
|
Minden állat |
||
Kiegészítő takarmányok – melaszos takarmányok |
|
|
|
||
|
Nyersrost |
Minden állat |
|
||
|
Összes cukor, szacharózban kifejezve |
Minden állat |
|
||
|
Nyershamu |
Minden állat |
|
||
|
Nyersolajok és zsírok |
|
Minden állat |
||
|
Kálcium |
|
Minden állat |
||
|
Foszfor |
|
Minden állat |
||
|
Nátrium |
|
Minden állat |
||
|
Kálium |
|
Minden állat |
||
|
Magnézium ≥ 0,5% |
Kérődzők |
Minden állat, a kérődzők |
||
|
<0,5% |
Minden állat |
|||
Kiegészítő takarmányok |
Nyersfehérje |
Állatok, kivéve – a macska és a kutya kivételével – a kedvtelésből tartott állatokat |
Kedvtelésből tartott állatok, a macska és a kutya kivételével |
||
|
Kálcium |
≥0,5% |
Állatok, kivéve a kedvtelésből tartott állatokat |
Kedvtelésből tartott állatok |
|
|
<0,5% |
Minden állat |
|||
|
Foszfor |
|
≥2% |
Állatok, kivéve a kedvtelésből tartott állatokat |
Kedvtelésből tartott állatok |
|
<2% |
Minden állat |
|||
|
Magnézium ≥0,5% |
Kérődzők |
Állatok, a kérődzők kivételével |
||
|
<0,5% |
Minden állat |
|||
|
Nátrium |
|
Minden állat |
||
|
Kálium |
|
Minden állat |
||
|
Energiaszint |
|
Baromfi, sertés, kérődzők |
||
|
Lizin |
Sertés |
Állatok, a sertés kivételével |
||
|
Metionin |
Baromfi |
Állatok, a baromfi kivételével |
||
|
Cisztin |
|
Minden állat |
||
|
Treonin |
|
Minden állat |
||
|
Triptofán |
|
Minden állat |
||
|
Keményítő |
|
Minden állat |
||
|
Összes cukor, szacharózban kifejezve |
|
Minden állat |
||
|
Összes cukor + keményítő |
|
Minden állat |
||
15. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez
|
Vizsgált paraméter |
Méréstartomány |
Eltérés |
|---|---|---|
|
Nedvesség |
c ≤5% |
± 0,4% A |
|
5% < c ≤ 10% |
± 8,0% R |
|
|
10% < c ≤ 20% |
± 0,8% A |
|
|
c > 20% |
± 4,0% R |
|
|
Nyersfehérje |
c ≤ 10% |
± 0,4% A |
|
10% < c ≤ 20% |
± 4,0% R |
|
|
c > 20% |
± 0,8% A |
|
|
Emészthető nyersfehérje |
c ≤ 10% |
± 0,8% A |
|
10% < c ≤ 20% |
± 10,0% R |
|
|
c > 20% |
± 2,0% A |
|
|
Nyers zsír |
c ≤ 5% |
± 0,4% A |
|
5% < c ≤ 15% |
± 8,0% R |
|
|
c > 15% |
± 1,2% A |
|
|
Nyers rost |
c ≤ 6% |
± 0,6% A |
|
6%< c ≤ 14% |
± 10% R |
|
|
c > 14% |
± 1,4% A |
|
|
Nyers hamu |
c ≤ 5% |
± 0,4% A |
|
5% < c ≤ 10% |
± 8,0% R |
|
|
10% < c ≤ 20% |
± 0,8% A |
|
|
c > 20% |
± 4,0% R |
|
|
Sósavban oldhatatlan hamu = homok |
c ≤ 3% |
± 0,3% A |
|
c > 3% |
± 10% R |
|
|
Oldhatósági index |
Teljes méréstartomány |
± 20% R |
|
Só (Cl- alapon) |
c ≤ 3% |
± 0,3% A |
|
c > 3% |
± 10% R |
|
|
Ca |
c ≤ 0,5% |
± 20% R |
|
0,5% < c ≤ 1% |
± 0,1% A |
|
|
1%< c ≤ 6% |
± 10% R |
|
|
6% < c ≤ 10% |
± 0,6% A |
|
|
c > 10% |
± 6% R |
|
|
K |
c ≤ 0,16% |
± 0,02% A |
|
0,16% < c ≤ 8% |
± 12,5% R |
|
|
c > 8% |
± 1,0% A |
|
|
Citromsavban, semleges és alkálikus ammónium-citrátban oldható foszfor |
c ≤ 5% |
± 16% R |
|
5% < c ≤ 10% |
± 0,8% A |
|
|
c > 10% |
± 10% R |
|
|
Karbonát |
c ≤ 6% |
± 10% R |
|
6% < c ≤ 10% |
± 0,6% A |
|
|
c > 10% |
± 6% R |
|
|
Mikroelemek I. |
c < 50 mg/kg |
± 30% R |
|
50 mg/kg < c ≤ 100 mg/kg |
± 15 mg/kg |
|
|
c > 100 mg/kg |
± 15% R |
|
|
Mikroelemek II. |
c ≤ 0,1 mg/kg |
± 60% R |
|
0,1 mg/kg < c ≤ 0,2 mg/kg |
± 0,06 mg/kg |
|
|
0,2 mg/kg < c ≤ 10 mg/kg |
± 30% R |
|
|
10 mg/kg < c ≤ 15 mg/kg |
± 3 mg/kg |
|
|
c > 15 mg/kg |
± 15% R |
|
|
Mikroelemek III. |
Teljes méréstartomány |
± 25% R |
|
Összes cukor, |
c ≤ 20% |
± 10% R |
|
c > 20% |
± 2% A |
|
|
Keményítő |
c ≤ 20% |
± 10% R |
|
c > 20% |
± 2% A |
|
|
Karbamid |
c ≤ 2% |
± 0,3% A |
|
c > 2% |
± 15% R |
|
|
Aminosav |
c ≤ 2% |
± 15% R |
|
2% < c ≤ 3% |
± 0,3% A |
|
|
3% < c ≤ 10% |
± 10% R |
|
|
10% < c ≤ 20% |
± 1% A |
|
|
20% < c ≤ 40% |
± 5% R |
|
|
40% < c ≤ 80% |
± 2% A |
|
|
c > 80% |
± 2,5% R |
|
|
Nitrát-nitrit |
Teljes méréstartomány |
± 15% R |
|
Karotin |
c ≤ 150 mg/kg |
± 20% R |
|
150 mg/kg < c ≤ 200 mg/kg |
± 30 mg/kg |
|
|
200 mg/kg < c ≤ 500 mg/kg |
± 15% R |
|
|
500 mg/kg < c ≤ 750 mg/kg |
± 75 mg/kg |
|
|
c > 750 mg/kg |
± 10% R |
|
|
A-vitamin |
c ≤ 10 000 NE/kg |
± 25% R |
|
10 000 NE/kg < c ≤ 20 000 NE/kg |
± 2500 NE/kg |
|
|
20 000 NE/kg < c ≤ 100 000 NE/kg |
± 12,5% R |
|
|
100 000 NE/kg < c ≤ 125 000 NE/kg |
± 12 500 NE/kg |
|
|
c > 125 000 NE/kg |
± 10% R |
|
|
D-vitamin |
c ≤ 1000 NE/kg |
± 60% R |
|
1000 NE/kg < c ≤ 1500 NE/kg |
± 600 NE/kg |
|
|
1500 NE/kg < c ≤ 5000 NE/kg |
± 40% R |
|
|
5000 NE/kg < c ≤ 8000 NE/kg |
± 2000 NE/kg |
|
|
8000 NE/kg < c ≤ 40 000 NE/kg |
± 25% R |
|
|
40 000 NE/kg < c ≤ 100 000 NE/kg |
± 10 000 NE/kg |
|
|
c >100 000 NE/kg |
± 10% R |
|
|
E-vitamin |
c ≤150 mg/kg |
± 20% R |
|
150 mg/kg < c ≤ 200 mg/kg |
± 30 mg/kg |
|
|
200 mg/kg < c ≤ 500 mg/kg |
± 15% R |
|
|
500 mg/kg < c ≤ 750 mg/kg |
± 75 mg/kg |
|
|
c > 750 mg/kg |
± 10% R |
|
|
K3-vitamin (menadion) |
c ≤ 5 mg/kg |
± 40% R |
|
5 mg/kg < c ≤ 10 mg/kg |
± 2 mg/kg |
|
|
10 mg/kg < c ≤ 100 mg/kg |
± 20% R |
|
|
100 mg/kg < c ≤ 160 mg/kg |
± 20 mg/kg |
|
|
160 mg/kg < c ≤ 400 mg/kg |
± 12,5% R |
|
|
400 mg/kg < c ≤ 500 mg/kg |
± 50 mg/kg |
|
|
c > 500 mg/kg |
± 10% R |
|
|
Egyéb vitaminok |
c ≤ 5 mg/kg |
± 40% R |
|
5 mg/kg < c ≤ 10 mg/kg |
± 2 mg/kg |
|
|
10 mg/kg < c ≤ 100 mg/kg |
± 20% R |
|
|
100 mg/kg < c ≤ 160 mg/kg |
± 20 mg/kg |
|
|
160 mg/kg < c ≤ 400 mg/kg |
± 12,5% R |
|
|
400 mg/kg < c ≤ 500 mg/kg |
± 50 mg/kg |
|
|
c > 500 mg/kg |
± 10% R |
|
|
Antioxidáns |
c ≤ 5 mg/kg |
± 30% R |
|
5 mg/kg < c ≤ 10 mg/kg |
± 1,5 mg/kg |
|
|
10 mg/kg < c ≤ 100 mg/kg |
± 15% R |
|
|
100 mg/kg < c ≤ 125 mg/kg |
± 15 mg/kg |
|
|
125 mg/kg < c ≤ 500 mg/kg |
± 12% R |
|
|
500 mg/kg < c ≤ 750 mg/kg |
± 60 mg/kg |
|
|
750 mg/kg < c ≤ 100 000 mg/kg |
± 8% R |
|
|
100 000 mg/kg < c ≤ 200 000 mg/kg |
± 8000 mg/kg |
|
|
200 000 mg/kg < c ≤ 400 000 mg/kg |
± 8% R |
|
|
400 000 mg/kg < c ≤ 800 000 mg/kg |
± 16 000 mg/kg |
|
|
c > 800 000 mg/kg |
± 2% R |
|
|
Állatgyógyászati |
c ≤ 5 mg/kg |
± 30% R |
|
5 mg/kg < c ≤ 10 mg/kg |
± 1,5 mg/kg |
|
|
10 mg/kg < c ≤ 100 mg/kg |
± 15% R |
|
|
100 mg/kg < c ≤ 125 mg/kg |
± 15 mg/kg |
|
|
125 mg/kg < c ≤ 500 mg/kg |
± 12% R |
|
|
500 mg/kg < c ≤ 750 mg/kg |
± 60 mg/kg |
|
|
750 mg/kg < c ≤ 100 000 mg/kg |
± 8% R |
|
|
100 000 mg/kg < c ≤ 200 000 mg/kg |
± 8000 mg/kg |
|
|
200 000 mg/kg < c ≤ 400 000 mg/kg |
± 8% R |
|
|
400 000 mg/kg < c ≤ 800 000 mg/kg |
± 16 000 mg/kg |
|
|
c > 800 000 mg/kg |
± 2% R |
|
|
Növényvédőszer-maradék |
c ≤ 0,1 mg/kg |
± 50% R |
|
0,1 mg/kg < c ≤ 0,2 mg/kg |
± 0,05 mg/kg |
|
|
c > 0,2 mg/kg |
± 25 % R |
|
|
Aflatoxin B1, B2, G1, G2 |
c ≤ 0,004 mg/kg |
± 50% R |
|
0,004 mg/kg < c ≤ 0,01 mg/kg |
± 0,002 mg/kg |
|
|
c > 0,01 mg/kg |
± 20% R |
|
|
|
|
|
|
|
|
|
|
Ochratoxin-A |
c ≤ 0,004 mg/kg |
± 50% R |
|
0,004 mg/kg < c ≤ 0,01 mg/kg |
± 0,002 mg/kg |
|
|
c > 0,01 mg/kg |
± 20% R |
|
|
Mikotoxinok |
c ≤ 0,1 mg/kg |
± 50% R |
|
0,1 mg/kg < c ≤ 0,2 mg/kg |
± 0,05 mg/kg |
|
|
0,2 mg/kg < c ≤ 1,0 mg/kg |
± 25% R |
|
|
1,0 mg/kg < c ≤ 2,5 mg/kg |
± 0,25 mg/kg |
|
|
c > 2,5 mg/kg |
± 10% R |
|
|
As |
c ≤ 1 mg/kg |
± 50% R |
|
1 mg/kg < c ≤ 2,5 mg/kg |
± 0,5 mg/kg |
|
|
2,5 mg/kg < c ≤ 15 mg/kg |
± 20% R |
|
|
15 mg/kg < c ≤ 30 mg/kg |
± 3,0 mg/kg |
|
|
c > 30 mg/kg |
± 10% R |
|
|
Hg |
c ≤ 0,06 mg/kg |
± 50% R |
|
0,06 mg/kg < c ≤ 0,1 mg/kg |
± 0,03 mg/kg |
|
|
0,1 mg/kg < c ≤ 0,2 mg/kg |
± 30% R |
|
|
0,2 mg/kg < c ≤ 0,3 mg/kg |
± 0,06 mg/kg |
|
|
c > 0,3 mg/kg |
± 20% R |
|
|
Cd |
c ≤ 0,2 mg/kg |
± 50% R |
|
0,2 mg/kg < c ≤ 0,4 mg/kg |
± 0,1 mg/kg |
|
|
0,4 mg/kg < c ≤ 1,0 mg/kg |
± 25% R |
|
|
1,0 mg/kg < c ≤ 2,5 mg/kg |
± 0,25 mg/kg |
|
|
c > 2,5 mg/kg |
± 10% R |
|
|
Pb |
c ≤ 5 mg/kg |
± 50% R |
|
3 mg/kg < c ≤ 5 mg/kg |
± 1,5 mg/kg |
|
|
5 mg/kg < c ≤ 10 mg/kg |
± 30% R |
|
|
10 mg/kg < c ≤ 20 mg/kg |
± 3 mg/kg |
|
|
20 mg/kg < c ≤ 40 mg/kg |
± 15% R |
|
|
40 mg/kg < c ≤ 60 mg/kg |
± 6 mg/kg |
|
|
c > 60 mg/kg |
± 10% R |
|
|
F |
c ≤ 60 mg/kg |
± 12 mg/kg |
|
60 mg/kg < c ≤ 500 mg/kg |
± 20% R |
|
|
500 mg/kg < c ≤ 1000 mg/kg |
± 100 mg/kg |
|
|
c > 1000 mg/kg |
± 10% R |
|
|
Csillagfürt alkaloida |
Teljes méréstartomány |
± 20% R |
|
Savszám, peroxidszám |
Teljes méréstartomány |
± 15% R |
|
Szabad zsírsavak, zsírsavösszeétel, illózsírsavak |
c ≤ 2% |
±15% R |
|
2%< c ≤ 3% |
± 0,3% A |
|
|
3%< c ≤ 10% |
± 10% R |
|
|
10%< c ≤ 20% |
± 1% A |
|
|
20%< c ≤ 40% |
± 5% R |
|
|
40%< c ≤ 80% |
± 2% A |
|
|
c > 80% |
± 2,5% R |
|
|
Ciánhidrogén |
Teljes méréstartomány |
± 20% R |
|
Szója és szójakészítmények tripszininhibitor aktivitása |
Teljes méréstartomány |
± 20% R |
|
Szója és szójakészítmények |
Teljes méréstartomány |
± 20% R |
|
Olajos magvak és darák ITC és VTO tartalma |
Teljes méréstartomány |
± 20% R |
|
Gossypol |
Teljes méréstartomány |
± 20% R |
|
Teobromin |
Teljes méréstartomány |
± 20% R |
16. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez
|
Sorszám: …….. |
Az Országos Mezőgazdasági Minősítő Intézet ezen igazolvánnyal rendelkező dolgozója a takarmányok előállításáról, forgalomba hozataláról és felhasználásáról szóló 2001. évi CXIX. törvény végrehajtásáról szóló 43/2003. (IV. 26.) FVM rendelet 30. §-a alapján beléphet a létesítmények és laboratóriumok területére, a létesítményre, a laboratóriumra, a takarmányokra, a vizsgálatokra vonatkozó nyilvántartásokat, dokumentációt megtekintheti, és azokról – az üzemi, illetve üzleti titok védelmére vonatkozó szabályok betartásával – másolatot készíthet, és az engedélyezési eljárás alatt álló új takarmányból térítésmentesen mintákat vehet. |
|
Az igazolvány tulajdonosának |
|
|
Sorszám: …….. |
Az Állatgyógyászati Oltóanyag-, Gyógyszer- és Takarmány-ellenőrző Intézet ezen igazolvánnyal rendelkező dolgozója a takarmányok előállításáról, forgalomba hozataláról és fel-használásáról szóló 2001. évi CXIX. törvény 11. §-a (3) bekezdésének i) pontja alapján beléphet a létesítmények területére, a takarmányokra vonatkozó nyilvántartásokat, dokumentációt megtekintheti, és azokról – az üzemi, illetve üzleti titok védelmére vonatkozó szabályok betartásával – másolatot készíthet. |
|
|
|
|
Sorszám: …….. |
Az Állomás ezen igazolvánnyal rendelkező dolgozója a takarmányok előállításáról, forgalomba hozataláról és felhasználásáról szóló 2001. évi CXIX. törvény |
|
Az igazolvány tulajdonosának |
|
17. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez75
|
|
Nedvesség |
Nyers hamu |
Nyers fehérje |
Nyers olajok, zsírok |
Nyers |
rost |
|---|---|---|---|---|---|---|
|
|
többlet |
többlet |
hiány |
hiány |
többlet |
hiány |
|
Tenyészsüldő, koca, kan |
6 |
7 |
13 |
0 |
6 |
6 |
|
Malac 30 kg-ig |
5 |
7 |
15 |
6 |
8 |
0 |
|
Hízósertés 30–60 kg |
5 |
7 |
10 |
6 |
6 |
0 |
|
Hízósertés 60 kg felett |
5 |
7 |
8 |
5 |
5 |
0 |
|
Szárnyas indító, nevelő (hízlaló) |
6 |
7 |
15 |
8 |
8 |
0 |
|
Szárnyas befejező |
6 |
7 |
10 |
8 |
8 |
0 |
|
Szárnyas jérce, tojó előkészítő |
6 |
7 |
8 |
0 |
5 |
0 |
|
Szárnyas tojó |
6 |
7 |
8 |
0 |
5 |
0 |
|
Egyéb szárnyas |
6 |
7 |
10 |
8 |
5 |
0 |
|
Borjú, bárány indító |
4 |
7 |
10 |
7 |
5 |
0 |
|
Kérődző, növendék, hízó |
4 |
7 |
6 |
7 |
0 |
0 |
|
Tehén, egyéb kérődző tenyészállat |
4 |
7 |
6 |
0 |
0 |
0 |
|
Egyéb kérődző |
4 |
7 |
6 |
6 |
0 |
0 |
|
Nyúl, egyéb prémes állat |
4 |
7 |
7 |
0 |
0 |
10 |
|
Ló |
5 |
7 |
7 |
0 |
5 |
0 |
|
Hal |
0 |
7 |
10 |
7 |
0 |
0 |
|
Kedvtelésből tartott állatok |
4 |
7 |
8 |
8 |
5 |
5 |
|
Egyéb állatok |
4 |
7 |
5 |
5 |
5 |
5 |
|
|
Energia |
Teljes |
cukor |
Karbamid-tartalom* |
Összes és hozzáadott aminósavak, aminósavanként |
Metionin- |
Na, K, Mg |
||
|---|---|---|---|---|---|---|---|---|---|
|
|
hiány |
hiány |
többlet |
hiány |
többlet |
hiány |
hiány |
hiány |
többlet |
|
Tenyészsüldő, koca, kan |
6 |
0 |
0 |
|
|
10 |
10 |
5 |
0 |
|
Malac 30 kg-ig |
6 |
0 |
0 |
|
|
13 |
13 |
6 |
8 |
|
Hízósertés 30–60 kg |
6 |
0 |
0 |
|
|
10 |
10 |
5 |
5 |
|
Hízósertés 60 kg felett |
6 |
0 |
0 |
|
|
7 |
7 |
5 |
0 |
|
Szárnyas indító, nevelő (hízlaló) |
13 |
5 |
5 |
|
|
13 |
13 |
6 |
6 |
|
Szárnyas befejező |
10 |
5 |
5 |
|
|
9 |
9 |
5 |
6 |
|
Szárnyas jérce, tojó előkészítő |
6 |
5 |
5 |
|
|
8 |
8 |
5 |
6 |
|
Szárnyas tojó |
6 |
5 |
5 |
|
|
8 |
8 |
5 |
7 |
|
Egyéb szárnyas |
6 |
5 |
5 |
|
|
8 |
8 |
5 |
6 |
|
Borjú, bárány indító |
5 |
0 |
0 |
5 |
10 |
7 |
7 |
5 |
0 |
|
Kérődző, növendék, hízó |
5 |
0 |
0 |
5 |
6 |
0 |
0 |
5 |
0 |
|
Tehén, egyéb kérődző tenyészállat |
5 |
0 |
0 |
5 |
6 |
0 |
0 |
5 |
0 |
|
Egyéb kérődző |
5 |
0 |
0 |
5 |
6 |
0 |
0 |
5 |
0 |
|
Nyúl, egyéb prémes állat |
5 |
0 |
0 |
|
|
6 |
6 |
5 |
0 |
|
Ló |
5 |
0 |
0 |
|
|
0 |
0 |
5 |
0 |
|
Hal |
5 |
0 |
0 |
|
|
8 |
8 |
5 |
0 |
|
Kedvtelésből tartott állatok |
5 |
0 |
0 |
|
|
7 |
7 |
5 |
5 |
|
Egyéb állatok |
5 |
0 |
0 |
|
|
5 |
5 |
5 |
5 |
|
|
Ca |
P |
Nyom-elemek, elemenként |
Vitaminok, |
Gyógyszertartalom, |
Egyéb garantált vizsgált hatóanyag, hatóanyagonként |
||
|---|---|---|---|---|---|---|---|---|
|
|
többlet/hiány |
többlet/hiány |
hiány |
hiány |
hiány |
többlet |
hiány |
többlet |
|
Tenyészsüldő, koca, kan |
5 |
5 |
8 |
10 |
13 |
15 |
5 |
5 |
|
Malac 30 kg-ig |
5 |
5 |
9 |
16 |
15 |
15 |
5 |
5 |
|
Hízósertés 30–60 kg |
5 |
5 |
8 |
10 |
10 |
10 |
5 |
5 |
|
Hízósertés 60 kg felett |
5 |
5 |
7 |
7 |
10 |
10 |
5 |
5 |
|
Szárnyas indító, nevelő (hízlaló) |
5 |
5 |
7 |
16 |
15 |
15 |
5 |
5 |
|
Szárnyas befejező |
5 |
5 |
5 |
10 |
10 |
10 |
5 |
5 |
|
Szárnyas jérce, tojó előkészítő |
5 |
5 |
6 |
11 |
5 |
15 |
5 |
5 |
|
Szárnyas tojó |
5 |
5 |
6 |
10 |
10 |
15 |
5 |
5 |
|
Egyéb szárnyas |
5 |
5 |
6 |
10 |
10 |
15 |
5 |
5 |
|
Borjú, bárány indító |
5 |
5 |
5 |
9 |
10 |
10 |
5 |
5 |
|
Kérődző, növendék, hízó |
5 |
5 |
5 |
5 |
8 |
8 |
5 |
5 |
|
Tehén, egyéb kérődző tenyészállat |
5 |
5 |
6 |
5 |
8 |
8 |
5 |
5 |
|
Egyéb kérődző |
5 |
5 |
5 |
5 |
8 |
8 |
5 |
5 |
|
Nyúl, egyéb prémes állat |
5 |
5 |
5 |
6 |
10 |
10 |
5 |
5 |
|
Ló |
5 |
5 |
5 |
6 |
15 |
15 |
5 |
5 |
|
Hal |
5 |
5 |
5 |
8 |
15 |
15 |
5 |
5 |
|
Kedvtelésből tartott állatok |
5 |
5 |
5 |
11 |
15 |
15 |
5 |
5 |
|
Egyéb állatok |
5 |
5 |
5 |
8 |
10 |
10 |
5 |
5 |
|
|
Mikro-biológia |
Salmonella |
Nemkívánatos |
Tiltott |
Avasság |
Megengedett maximális értéket meghaladó adalék-anyagok, adalék-anyagonként |
Összetételben nem szereplő nem mérgező anyagok, |
|---|---|---|---|---|---|---|---|
|
Tenyészsüldő, koca, kan |
15 |
61 |
61 |
61 |
10 |
31 |
10 |
|
Malac 30 kg-ig |
15 |
61 |
61 |
61 |
10 |
31 |
15 |
|
Hízósertés 30–60 kg |
10 |
61 |
61 |
61 |
8 |
31 |
10 |
|
Hízósertés 60 kg felett |
10 |
61 |
61 |
61 |
8 |
31 |
10 |
|
Szárnyas indító, nevelő (hízlaló) |
20 |
61 |
61 |
61 |
15 |
31 |
15 |
|
Szárnyas befejező |
15 |
61 |
61 |
61 |
15 |
31 |
15 |
|
Szárnyas jérce, tojó előkészítő |
15 |
61 |
61 |
61 |
10 |
31 |
15 |
|
Szárnyas tojó |
15 |
61 |
61 |
61 |
10 |
31 |
15 |
|
Egyéb szárnyas |
15 |
61 |
61 |
61 |
10 |
31 |
15 |
|
Borjú, bárány indító |
10 |
61 |
61 |
61 |
8 |
31 |
10 |
|
Kérődző, növendék, hízó |
8 |
61 |
61 |
61 |
7 |
31 |
5 |
|
Tehén, egyéb kérődző tenyészállat |
8 |
61 |
61 |
61 |
7 |
31 |
8 |
|
Egyéb kérődző |
8 |
61 |
61 |
61 |
7 |
31 |
5 |
|
Nyúl, egyéb prémes állat |
10 |
61 |
61 |
61 |
8 |
31 |
8 |
|
Ló |
15 |
61 |
61 |
61 |
10 |
31 |
10 |
|
Hal |
5 |
61 |
61 |
61 |
8 |
31 |
5 |
|
Kedvtelésből tartott állatok |
10 |
61 |
61 |
61 |
15 |
31 |
10 |
|
Egyéb állatok |
10 |
61 |
61 |
61 |
8 |
31 |
8 |
|
Vizsgálati paraméterek |
|
Hibapont |
|---|---|---|
|
|
|
|
|
Nedvesség |
többlet |
7 |
|
Nyers hamu |
többlet |
6 |
|
|
hiány |
5 |
|
Nyers fehérje |
hiány |
15 |
|
|
többlet |
5 |
|
Emészthető nyers fehérje |
hiány |
15 |
|
Nyers olajok, zsírok |
hiány |
7 |
|
|
többlet |
5 |
|
Nyers rost |
többlet |
5 |
|
|
hiány |
8 |
|
Karbamid |
hiány |
5 |
|
|
többlet |
15 |
|
Keményítő |
hiány |
7 |
|
|
többlet |
5 |
|
Összes és hozzáadott aminósavak aminósavanként |
hiány |
15 |
|
Metionin-Hidroxi-Analóg |
hiány |
15 |
|
Nátrium, Kálium, Magnézium elemenként |
hiány |
6 |
|
|
többlet |
8 |
|
Kálcium |
hiány |
9 |
|
|
többlet |
5 |
|
Foszfor |
hiány |
9 |
|
|
többlet |
5 |
|
Sósavban oldhatatlan hamu |
többlet |
8 |
|
Nyomelemek, nyomelemenként |
hiány |
10 |
|
Vitaminok, vitaminonként |
hiány |
15 |
|
Egyéb garantált, vizsgált hatóanyag, hatóanyagonként |
hiány |
5 |
|
|
többlet |
5 |
|
Mikrobiológia (Salmonella nélkül) |
|
25 |
|
Salmonella |
|
61 |
|
Nemkívánatos anyagok, anyagonként |
|
61 |
|
Maximális mértéket meghaladó adalékanyagok, adalékanyagonként |
|
25 |
|
Avasság |
|
25 |
|
Tiltott anyagok, anyagonként |
|
61 |
|
Összetételben nem szereplő, nem mérgező anyagok, |
|
15 |
18. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez76
|
Vizsgálati paraméter |
Sávhatárok |
Megengedhető eltérések |
|---|---|---|
|
Nedvesség |
≤ 5,00% |
+ 0,50 A% |
|
5,00 – 10,00% |
+ 10,00 R% |
|
|
10,00 – 20,00% |
+ 1,00 A% |
|
|
≥ 20,00% |
+ 5,00 R% |
|
|
Nyers hamu |
≤ 5,00% |
+ 0,50 A% |
|
5,00 – 10,00% |
+ 10,00 R% |
|
|
≥ 10,00% |
+ 1,00 A% |
|
|
Nyers fehérje |
≤ 10,00% |
– 1,00 A% |
|
10,00 – 20,00% |
– 10,00 R% |
|
|
≥ 20,00% |
– 2,00 A% |
|
|
Emészthető nyers |
≤ 15,00% |
– 1,80 A% |
|
15,00 – 25,00% |
– 12,00 R% |
|
|
≥ 25,00% |
– 3,00 A% |
|
|
Nyers olajok és zsírok |
≤ 8,00% |
– 0,80 A% |
|
8,00 – 15,00% |
– 10,00 R% |
|
|
≥ 15,00% |
– 1,50 A% |
|
|
Teljes (össz) cukor |
≤ 10,00% |
– 1,00 A% |
|
10,00 – 20,00% |
– 10,00 R% |
|
|
≥ 20,00% |
– 2,00 A% |
|
|
Karbamidtartalom |
≤ 2,00% |
– 0,50 A% |
|
≥ 2,00% |
– 25,00 R% |
|
|
Keményítő |
≤ 10,00% |
– 1,00 A% |
|
10,00 – 25,00% |
– 10,00 R% |
|
|
≥ 25,00% |
– 2,50 A% |
|
|
Nyers rost |
≤ 6,00% |
± 1, 5 A% |
|
6,00 – 12,00% |
± 25,00 R% |
|
|
≥ 12,00% |
± 3, 00 A% |
|
|
Összes |
|
– 20,00 R% |
|
Összes és hozzáadott Cisztin |
|
– 20,00 R% |
|
Összes és hozzáadott Triptofán |
|
– 15,00 R% |
|
Metionin-Hidroxi-Analóg |
|
– 15,00 R% |
|
Nátrium, Kálium, Magnézium |
≤ 0,70% |
– 0,10 A% |
|
0,70 – 5,00% |
– 15,00 R% |
|
|
5,00 – 7,50% |
– 0,75 A% |
|
|
7,50 – 15,00% |
– 10,00 R% |
|
|
≥ 15,00% |
– 1,50 A% |
|
|
Kálcium, Foszfor |
≤ 1,00% |
± 0,30 A% |
|
1,00 – 2,00% |
± 30,00 R% |
|
|
2,00 – 5,00% |
± 0,60 A% |
|
|
≥ 5,00% |
± 12,00 A% |
|
|
Sósavban oldhatatlan |
≤ 4,00% |
+ 0,40 A% |
|
4,00 – 10,00% |
+ 10,00 R% |
|
|
≥10,00% |
+ 1,00 A% |
|
|
Energiatartalom |
≤ 10,00 MJ/kg |
– 10,00 R% |
|
≥ 10,00 MJ/kg |
– 1,00 A% |
|
|
Nyomelemtartalom |
≤ 30,00 mg/kg |
– 15,00 mg/kg A |
|
30,00 mg/kg – 50,00 mg/kg |
– 50,00 R% |
|
|
50,00 mg/kg – 100,00 mg/kg |
– 25,00 mg/kg A |
|
|
≥ 100,00 mg/kg |
– 25,00 R% |
|
|
Szeléntartalom |
≤ 0,50 mg/kg |
– 70,00 R% |
|
0,50 mg/kg – 1,00 mg/kg |
– 0,35 mg/kg A |
|
|
1,00 mg/kg – 10,00 mg/kg |
– 35,00 R% |
|
|
10,00 mg/kg – 14,00 mg/kg |
– 3,50 mg/kg A |
|
|
≥ 14,00 mg/kg |
– 25,00 R% |
|
|
Jódtartalom |
|
– 40,00 R% |
|
A-vitamintartalom |
≤ 10.000,00 NE/kg |
– 40,00 R% |
|
10.000,00 NE/kg – 20.000,00 NE/kg |
– 4.000,00 NE/kg A |
|
|
20.000,00 NE/kg – 100.000,00 NE/kg |
– 20,00 R% |
|
|
100.000,00 NE/kg – 125.000,00 NE/kg |
– 20.000,00 NE/kg A |
|
|
≥ 125.000,00 NE/kg |
– 16,00 R% |
|
|
D-vitamin csoport |
≤ 3.000,00 NE/kg |
– 70,00 R% |
|
3.000,00 NE/kg – 6.000,00 NE/kg |
– 2.100,00 NE/kg A |
|
|
6.000,00 NE/kg – 60.000,00 NE/kg |
– 35,00 R% |
|
|
60.000,00 NE/kg – 100.000,00 NE/kg |
– 21.000,00 NE/kg A |
|
|
≥ 100.000,00 NE/kg |
– 21,00 R% |
|
|
E-vitamin-acetát- |
≤ 150,00 mg/kg |
– 30,00 R% |
|
150,00 mg/kg – 180,00 mg/kg |
– 45,00 mg/kg A |
|
|
180,00 mg/kg – 400,00 mg/kg |
– 25,00 R% |
|
|
400,00 mg/kg – 800,00 mg/kg |
– 100,00 mg/kg A |
|
|
≥ 800,00 mg/kg |
– 12,50 R% |
|
|
K3 –vitamin- |
≤ 40,00 mg/kg |
– 50,00 R% |
|
40,00 mg/kg – 50,00 mg/kg |
– 20,00 mg/kg A |
|
|
50,00 mg/kg – 100,00 mg/kg |
– 40,00 R% |
|
|
100,00 mg/kg – 200,00 mg/kg |
– 40,00 mg/kg A |
|
|
≥ 200,00 mg/kg |
– 20,00 R% |
|
|
Egyéb vitamin- |
≤ 5,00 mg/kg |
– 50,00 R% |
|
5,00 mg/kg – 10,00 mg/kg |
– 2,50 mg/kg A |
|
|
10,00 mg/kg – 100,00 mg/kg |
– 25,00 R% |
|
|
100,00 mg/kg – 125,00 mg/kg |
– 25,00 mg/kg A |
|
|
125,00 mg/kg – 500,00 mg/kg |
– 20,00 R% |
|
|
500,00 mg/kg – 800,00 mg/kg |
– 100,00 mg/kg A |
|
|
≥ 800,00 mg/kg |
– 12,50 R% |
|
|
Probiotikumok, enzimek |
|
± 10,00 R% |
|
Gyógyszer- |
≤ 5,00 mg/kg |
± 40,00 R% |
|
Egyéb, a mellékletben nem szereplő garantált, valamint vizsgált hatóanyag-tartalom |
|
|
19. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez77
|
Vizsgálati paraméter |
Sávhatárok |
Megengedhető eltérések |
|---|---|---|
|
Nedvesség |
≤ 20,00% |
+ 1,50 A% |
|
20,00 – 40,00% |
+ 7,50 R% |
|
|
≥ 40,00% |
+ 3,00 A% |
|
|
Nyers hamu |
|
+ 1,50 A% |
|
Nyers fehérje |
≤ 12,50% |
– 2,00 A% |
|
12,50 – 20,00% |
– 16,00 R% |
|
|
≥ 20,00% |
– 3,20 A% |
|
|
Nyers olajok és zsírok |
|
– 2,50 A% |
|
Teljes (össz) cukor |
≤ 10,00% |
– 1,00 A% |
|
10,00 – 20,00% |
– 10,00 R% |
|
|
≥ 20,00% |
– 2,00 A% |
|
|
Keményítő |
≤ 10,00% |
– 1,00 A% |
|
10,00 – 25,00% |
– 10,00 R% |
|
|
≥25,00% |
– 2,50 A% |
|
|
Nyers rost |
|
+ 1,00 A% |
|
Összes, hozzáadott Lizin, Metionin, Treonin |
|
– 15,00 R% |
|
Összes és hozzáadott Cisztin, Triptofán |
|
– 20,00 R% |
|
Metionin-Hidroxi-Analóg |
|
– 15,00 R% |
|
Nátrium, Kálium, Magnézium |
≤ 0,70% |
– 0,10 A% |
|
0,70 – 5,00% |
– 15,00 R% |
|
|
5,00 – 7,50% |
– 0,75 A% |
|
|
7,50 – 15,00% |
– 10,00 R% |
|
|
≥ 15,00% |
– 1,50 A% |
|
|
Kálcium, Foszfor |
≤ 1,00% |
– 0,15 A% |
|
1,00 – 6,00% |
– 15,00 R% |
|
|
6,00 – 12,00% |
– 0,90 A% |
|
|
12,00 – 16,00% |
– 7,50 R% |
|
|
≥ 16,00% |
– 1,20 A% |
|
|
Sósavban oldhatatlan |
≤ 4,00% |
+ 0,40 A% |
|
4,00 – 10,00% |
+ 10,00 R% |
|
|
≥10,00% |
+ 1,00 A% |
|
|
Energiatartalom |
≤ 10,00 MJ/kg |
– 10,00 R% |
|
≥ 10,00 MJ/kg |
– 1,00 A% |
|
|
Nyomelemtartalom |
≤ 30,00 mg/kg |
– 15,00 mg/kg A |
|
30,00 mg/kg – 50,00 mg/kg |
– 50,00 R% |
|
|
50,00 mg/kg – 100,00 mg/kg |
– 25,00 mg/kg A |
|
|
≥ 100,00 mg/kg |
– 25,00 R% |
|
|
Szeléntartalom |
≤ 0,50 mg/kg |
– 70,00 R% |
|
0,50 mg/kg – 1,00 mg/kg |
– 0,35 mg/kg A |
|
|
1,00 mg/kg – 10,00 mg/kg |
– 35,00 R% |
|
|
10,00 mg/kg – 14,00 mg/kg |
– 3,50 mg/kg A |
|
|
≥ 14,00 mg/kg |
– 25,00 R% |
|
|
Jódtartalom |
|
– 40,00 R% |
|
A-vitamintartalom |
≤ 10.000,00 NE/kg |
– 40,00 R% |
|
10.000,00 NE/kg – 20.000,00 NE/kg |
– 4.000,00 NE/kg A |
|
|
20.000,00 NE/kg – 100.000,00 NE/kg |
– 20,00 R% |
|
|
100.000,00 NE/kg – 125.000,00 NE/kg |
– 20.000,00 NE/kg A |
|
|
≥ 125.000,00 NE/kg |
– 16,00 R% |
|
|
D-vitamin csoport |
≤ 3.000,00 NE/kg |
– 70,00 R% |
|
3.000,00 NE/kg – 6.000,00 NE/kg |
– 2.100,00 NE/kg A |
|
|
6.000,00 NE/kg – 60.000,00 NE/kg |
– 35,00 R% |
|
|
60.000,00 NE/kg – 100.000,00 NE/kg |
– 21.000,00 NE/kg A |
|
|
≥ 100.000,00 NE/kg |
– 21,00 R% |
|
|
E-vitamin-acetát- |
≤ 150,00 mg/kg |
– 30,00 R% |
|
150,00 mg/kg – 180,00 mg/kg |
– 45,00 mg/kg A |
|
|
180,00 mg/kg – 400,00 mg/kg |
– 25,00 R% |
|
|
400,00 mg/kg – 800,00 mg/kg |
– 100,00 mg/kg A |
|
|
≥ 800,00 mg/kg |
– 12,50 R% |
|
|
K3 -vitamin- |
≤ 40,00 mg/kg |
– 50,00 R% |
|
40,00 mg/kg – 50,00 mg/kg |
– 20,00 mg/kg A |
|
|
50,00 mg/kg – 100,00 mg/kg |
– 40,00 R% |
|
|
100,00 mg/kg – 200,00 mg/kg |
– 40,00 mg/kg A |
|
|
≥ 200,00 mg/kg |
– 20,00 R% |
|
|
Egyéb vitamin |
≤ 5,00 mg/kg |
– 50,00 R% |
|
5,00 mg/kg – 10,00 mg/kg |
– 2,50 mg/kg A |
|
|
10,00 mg/kg – 100,00 mg/kg |
– 25,00 R% |
|
|
100,00 mg/kg – 125,00 mg/kg |
– 25,00 mg/kg A |
|
|
125,00 mg/kg – 500,00 mg/kg |
– 20,00 R% |
|
|
500,00 mg/kg – 800,00 mg/kg |
– 100,00 mg/kg A |
|
|
≥ 800,00 mg/kg |
– 12,50 R% |
|
|
Probiotikum, enzim |
|
± 10,00 R% |
|
Egyéb, a mellékletben nem szereplő garantált, valamint vizsgált hatóanyag-tartalom |
|
|
20. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez78
21. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez79
22. számú melléklet a 43/2003. (IV. 26.) FVM rendelethez80
|
Maximális elem-mennyiség teljes értékű takarmány kg-onként |
||
|---|---|---|
|
A. |
||
|
|
|
|
|
B. |
||
|
1. Jód |
lófélék (összesen) |
4 mg/kg |
|
|
halak (összesen) |
20 mg/kg |
|
|
egyéb állatfajok (összesen) |
10 mg/kg |
|
2. Molibdén |
minden állatfaj (összesen) |
2,5 mg/kg |
|
3. Szelén |
minden állatfaj (összesen) |
0,5 mg/kg |
A rendeletet a 65/2012. (VII. 4.) VM rendelet 48. § a) pontja hatályon kívül helyezte 2012. július 18. napjával. Alkalmazására lásd e hatályon kívül helyező rendelet 46. §-át.
A Vhr. 1. §-ának 2. pontja a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A Vhr. 1. §-ának 5. pontja a 21/2004. (II. 27.) FVM rendelet 1. § (1) bekezdésével megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 1. §-ának 22. pontját a 21/2004. (II. 27.) FVM rendelet 1. § (2) bekezdése iktatta be, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 1. §-ának 23. pontját a 21/2004. (II. 27.) FVM rendelet 1. §-ának (3) bekezdése iktatta be.
A 2. § (1) bekezdése a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A 2. § (2) bekezdése a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A 3. § (1) bekezdése a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A 4. §-t a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja hatályon kívül helyezte. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
Az 5. § (1) bekezdésének bevezető szövegrésze a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A Vhr. 5. §-a (1) bekezdésének b) pontját a 21/2004. (II. 27.) FVM rendelet 20. § (3) bekezdése hatályon kívül helyezte.
Az 5. § (1) bekezdésének i) pontját a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja hatályon kívül helyezte. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
Az 5. § (3) bekezdése a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A 6. § a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A Vhr. 7. §-ának (5) bekezdése a 45. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A Vhr. 7. §-ának (6) bekezdése a 45. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A Vhr. 7. §-ának (8) bekezdését a 21/2004. (II. 27.) FVM rendelet 2. §-a iktatta be, e módosító rendelet 20. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A Vhr. 7. §-ának (9) bekezdését a 21/2004. (II. 27.) FVM rendelet 2. §-a iktatta be, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 7. §-ának (10) bekezdését a 21/2004. (II. 27.) FVM rendelet 2. §-a iktatta be, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 7. §-ának (11) bekezdését a 21/2004. (II. 27.) FVM rendelet 2. §-a iktatta be, e módosító rendelet 20. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A Vhr. 8. §-ának (2) bekezdése a 21/2004. (II. 27.) FVM rendelet 3. §-ával megállapított szöveg.
A Vhr. 9. §-ának (3) bekezdését a 21/2004. (II. 27.) FVM rendelet 4. §-a iktatta be.
A Vhr. 11. §-a a 21/2004. (II. 27.) FVM rendelet 5. §-ával megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 11/A. §-át a 21/2004. (II. 27.) FVM rendelet 6. §-a iktatta be, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 11/A. §-ának (1) bekezdése szerinti nyilvántartást – a 21/2004. (II. 27.) FVM rendelet 20. § (4) bekezdése alapján – az Állomás első ízben 2004. március 20-ig köteles megküldeni az ÁOGYTI-nek. Az ÁOGYTI az Állomások nyilvántartásai alapján, a minisztérium útmutatása szerint 2004. április 1-jéig készíti el a takarmány-előállító üzemek országos nyilvántartását.
A Vhr. 11/A. §-ának (5) bekezdése a 21/2004. (II. 27.) FVM rendelet 20. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A 12. § (2) bekezdése a 45. § (4) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésével egyidejűleg hatályát vesztette.
A Vhr. 15. §-ának (2) bekezdése a 21/2004. (II. 27.) FVM rendelet 7. §-ával megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 15. §-ának (3) bekezdése a 21/2004. (II. 27.) FVM rendelet 7. §-ával megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 15. §-ának (4) bekezdése a 21/2004. (II. 27.) FVM rendelet 7. §-ával megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 17. §-ának (1) bekezdése a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A Vhr. 17. §-a (2) bekezdésének e) pontja a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A Vhr. 18. §-a a 11/2007. (II. 20.) FVM rendelet 1. §-ával megállapított szöveg.
A Vhr. 19. §-a a 21/2004. (II. 27.) FVM rendelet 9. §-ával megállapított szöveg.
A Vhr. 19. §-ának (1) bekezdése a 11/2007. (II. 20.) FVM rendelet 2. §-ával megállapított szöveg.
A Vhr. 19. §-ának (2) bekezdése a 11/2007. (II. 20.) FVM rendelet 2. §-ával megállapított szöveg.
A Vhr. 19/A. §-át a 21/2004. (II. 27.) FVM rendelet 10. §-a iktatta be, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 22. §-a a 11/2007. (II. 20.) FVM rendelet 3. §-ával megállapított szöveg. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 22/A. §-át a 11/2007. (II. 20.) FVM rendelet 3. §-a iktatta be. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 22/B. §-át a 11/2007. (II. 20.) FVM rendelet 3. §-a iktatta be. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 22/C. §-át a 11/2007. (II. 20.) FVM rendelet 3. §-a iktatta be. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 22/D. §-át a 11/2007. (II. 20.) FVM rendelet 3. §-a iktatta be. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 22/E. §-át a 11/2007. (II. 20.) FVM rendelet 3. §-a iktatta be. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 23. §-ának (2) bekezdését a 11/2007. (II. 20.) FVM rendelet 8. § (1) bekezdésének a) pontja hatályon kívül helyezte.
A Vhr. 24. §-ának (1) bekezdése a 11/2007. (II. 20.) FVM rendelet 4. §-ával megállapított szöveg. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 24. §-ának (4) bekezdése a 21/2004. (II. 27.) FVM rendelet 12. §-ával megállapított szöveg.
A Vhr. 25. §-ának (2) bekezdése a 45. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A Vhr. 25. §-ának (3) bekezdése a 45. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba. A Vhr. 25. §-ának (3) bekezdése a 11/2007. (II. 20.) FVM rendelet 5. §-ával megállapított szöveg.
A Vhr. 25. §-ának (5) bekezdése a 45. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A Vhr. 29. §-át a 11/2007. (II. 20.) FVM rendelet 8. § (1) bekezdésének a) pontja hatályon kívül helyezte.
A Vhr. 31. §-ának (3) bekezdése a 45. § (2) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésének napján lépett hatályba.
A Vhr. 33. §-a (1) bekezdése a) pontjának 4. alpontja a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A Vhr. 33. §-a (1) bekezdése d) pontjának 3. alpontja a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A 36. § a 45. § (4) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésével egyidejűleg hatályát vesztette.
A Vhr. 38. §-ának (1) bekezdése a 21/2004. (II. 27.) FVM rendelet 13. § (1) bekezdésével megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 38. §-a (3) bekezdésének c) pontja a 21/2004. (II. 27.) FVM rendelet 13. § (2) bekezdésével megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 38. §-a (4) bekezdésének b) pontja a 21/2004. (II. 27.) FVM rendelet 13. § (3) bekezdésével megállapított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 39. §-a (1) bekezdésének e) pontját a 21/2004. (II. 27.) FVM rendelet 14. §-a iktatta be, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 40. §-ának (1) bekezdése a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A Vhr. 40. §-ának (3) bekezdése a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A Vhr. 40. §-a (4) bekezdésének a) pontja a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A Vhr. 41. §-a a 11/2007. (II. 20.) FVM rendelet 7. § a) pontja szerint módosított szöveg.
A 42–44. §-t a 194/2008. (VII. 31.) Korm. rendelet 13. § (2) bekezdésének b) pontja hatályon kívül helyezte azzal, hogy a 2008. szeptember 1. napját megelőzően elkövetett jogsértések esetén még a hatályon kívül helyezett rendelkezéseket kell alkalmazni.
A Vhr. 45. §-ának (3) bekezdését a 118/2008. (V. 8.) Korm. rendelet 9. §-ának 285. pontja hatályon kívül helyezte.
A Vhr. 45. §-ának (4) bekezdése a 21/2004. (II. 27.) FVM rendelet 16. §-ával megállapított szöveg.
A 45. § (5) bekezdését a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja hatályon kívül helyezte. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A Vhr. 45. §-ának (7) bekezdését a 118/2008. (V. 8.) Korm. rendelet 9. §-ának 285. pontja hatályon kívül helyezte.
A Vhr. 46. §-a a 11/2007. (II. 20.) FVM rendelet 6. §-ával megállapított szöveg.
A Vhr. 1. számú melléklete a 21/2004. (II. 27.) FVM rendelet 17. §-a, a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. Ez utóbbi módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A 2. számú melléklet a 362/2008. (XII. 31.) Korm. rendelet 44. § (2) bekezdésének 47. pontja szerint módosított szöveg. E módosító rendelet 45. § (1) bekezdése alapján a rendelkezést a 2009. március 1. napját követően indult eljárásokban kell alkalmazni.
A Vhr. 3. számú melléklete a 11/2007. (II. 20.) FVM rendelet 7. § b) pontja szerint módosított szöveg. E módosító rendelet 8. § (2) bekezdése alapján a 2007. március 7. napja előtt gyártott, a gyártás idején hatályos jogszabályi előrásoknak megfelelő jelöléssel ellátott csomagolóeszközök, címkék 2007. május 31-ig, és az ezen csomagolóeszközzel, címkével forgalomba hozott termékek a minőségmegőrzési idő lejártáig használhatóak fel.
A Vhr. 4. számú melléklete a 11/2007. (II. 20.) FVM rendelet 7. § b) pontja szerint módosított szöveg.
A 6–13. számú melléklet a 45. § (4) bekezdése alapján a Magyar Köztársaságnak az Európai Unióhoz történő csatlakozásáról szóló nemzetközi szerződést kihirdető törvény hatálybalépésével egyidejűleg hatályát vesztette.
A Vhr. 14. számú melléklete a 21/2004. (II. 27.) FVM rendelet 17. §-a, a 11/2007. (II. 20.) FVM rendelet 8. § (1) bekezdésének a) pontja szerint módosított szöveg.
A Vhr. 17. számú melléklete a 21/2004. (II. 27.) FVM rendelet 17. §-a szerint módosított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 18. számú melléklete a 21/2004. (II. 27.) FVM rendelet 17. §-a, a 11/2007. (II. 20.) FVM rendelet 8. § (1) bekezdésének a) pontja szerint módosított szöveg.
A Vhr. 19. számú melléklete a 11/2007. (II. 20.) FVM rendelet 8. § (1) bekezdésének a) pontja szerint módosított szöveg.
A Vhr. 20. számú melléklete a 21/2004. (II. 27.) FVM rendelet 17. §-a szerint módosított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 21. számú melléklete a 21/2004. (II. 27.) FVM rendelet 17. §-a szerint módosított szöveg, e módosító rendelet 20. § (1) bekezdése alapján a rendelkezést a 2004. március 13-át követően indult eljárásokban kell alkalmazni.
A Vhr. 22. számú melléklete a 21/2004. (II. 27.) FVM rendelet 17. §-ával megállapított és e módosító rendelet 20. § (3) bekezdése szerint módosított szöveg.
- Hatályos
- Már nem hatályos
- Még nem hatályos
- Módosulni fog
- Időállapotok
- Adott napon hatályos
- Közlönyállapot
- Indokolás



